4 Tipos de anticuerpos monoclonales
Tabla de Contenidos
Los anticuerpos monoclonales sirven como herramientas críticas en inmunología, biología molecular, biología celular y medicina traslacional. Su agrupación estructural juega un papel directo en la fiabilidad de las pruebas, el riesgo de reacción inmune, la facilidad de aprobación y las posibilidades de tratamiento posterior. Al elegir un estilo de anticuerpo monoclonal, los científicos necesitan comprobar la precisión del antígeno, los números de fuerza de unión, las formas de localización de epítopos, la reacción cruzada y la respuesta inmune del huésped. También deben pensar en hacer horarios y configuraciones de control de calidad que guíen los resultados repetidos. Beijing Solarbio Ciencia y Tecnología Co., Ltd. Ha trabajado en el área de reactivos de ciencias de la vida desde 2004. Actúa como una empresa nacional de alta tecnología que integra I+ D, producción, ventas y servicio. La compañía ha establecido una plataforma completa que cubre anticuerpos, proteínas recombinantes, kits de ELISA, kits de ensayo bioquímico, soluciones de tinción, estándares analíticos, péptidos y compuestos de moléculas pequeñas. La empresa tiene ISO 9001, ISO 13485Certificaciones ISO 14001 y ISO 45001. Ha respaldado casi 150.000 publicaciones importantes, que incluyen artículos en revistas como NATURE MEDICINE, CELL y CELL RESEARCH. Esto muestra el crecimiento técnico y la calidad de repetición de sus productos inmunes.
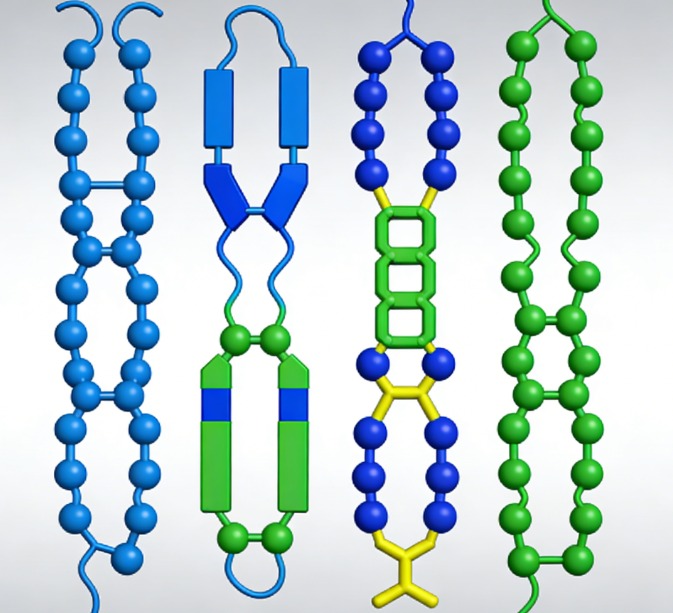
Tipo 1Anticuerpos monoclonales murinos
Los anticuerpos monoclonales murinos son el formato de anticuerpo derivado del hibridoma más antiguo. Todavía se utilizan ampliamente en la investigación básica y la validación de antígenos en etapas tempranas, debido a su alta especificidad y protocolos de producción maduros.
Características de los anticuerpos monoclonales murinos
Anticuerpos monoclonales murinos inmunizando ratones BALB/c con proteínas purificadas o antígenos péptidos sintéticos. A continuación, se recogieron de los ratones inmunizados y se fusionaron con células de mieloma (por ejemplo, SP2/0) a una relación definida, para generar líneas celulares de hibridoma estables que secretan moléculas de inmunoglobulina homogéneas. Estos anticuerpos contienen regiones variables murinas completas (Fv) y regiones constantes (Fc), que confieren una alta afinidad de unión a los epítopos diana, incluyendo tanto epítopos lineales como conformacionales, siempre que se usen adyuvantes apropiados para mantener la conformación espacial nativa del antígeno.
Los laboratorios típicamente seleccionan los títulos de anticuerpos séricos mediante ELISA basado en proteínas antes de la fusión celular. Las líneas de hibridoma positivos se someten a múltiples rondas de subclonación para obtener líneas celulares monoclonales estables, seguidas de producción de sobrenadante de cultivo y purificación de afinidad de anticuerpos.
Aplicaciones y limitaciones técnicas
Los anticuerpos monoclonales murinos se ajustan bien para la transferencia Western (WB), la inmunohistoquímica (IHC), la tinción por inmunofluorescencia (IF), la cuantificación por ELISA y el mapeo de epítopos en la investigación en etapa temprana. Sin embargo, la estructura de inmunoglobulina murina completa puede inducir una fuerte respuesta de anticuerpo anti-ratón humano (HAMA).
Desarrollo estructurado a través de servicios de anticuerpos personalizados
La Plataforma de Servicio de Anticuerpos Personalizados proporciona servicios de desarrollo de anticuerpos monoclonales de ratón personalizados de extremo a extremo, incluyendo inmunización de ratones BALB/c, detección de títulos de anticuerpos séricos basados en ELISA, fusión de esplenocitos, cribado sobrenadante, subclonación, establecimiento de línea celular monoclonal estable y purificación de anticuerpos.
La preparación rápida del antisuero puede completarse dentro de 3-4 semanas para aplicaciones en las que solo se requiere antisuero policlonal. El desarrollo completo de anticuerpos monoclonales normalmente dura varios meses, dependiendo del rendimiento de cribado y los requisitos de validación. La dosificación de antígeno requerida es relativamente baja: típicamente, 300-500 μg de antígeno purificado son suficientes para la inmunización de 5 ratones BALB/c, lo que reduce en gran medida el consumo de proteínas recombinantes preciosas y péptidos sintéticos.
Tipo 2Anticuerpos monoclonales quiméricos
Cuando la reacción inmune se convierte en una preocupación en la investigación translacional, los anticuerpos monoclonales quiméricos proporcionan un formato estructural intermedio que equilibra una alta especificidad de unión al antígeno con un riesgo de inmunogenicidad reducido.
Los anticuerpos monoclonales quiméricos conservan las regiones variables murinas responsables del reconocimiento de antígenos, mientras sustituyen las regiones constantes murinas por regiones constantes de inmunoglobulina humana. Este diseño aumenta la proporción global de secuencia humana en el anticuerpo, reduciendo de este modo significativamente la inmunogenicidad.
Diseño estructural y consideraciones inmunológicas
La unión al antígeno se encuentra en las regiones de cadena variable pesada (VH) y variable ligera (VL). La retención de estas regiones preserva completamente la especificidad del epítopo, mientras que el reemplazo de las regiones constantes con secuencias derivadas del ser humano modula las funciones del efector inmune mediadas por Fc y las características de la vida media en suero del anticuerpo. En comparación con las inmunoglobulinas murinas completas, esta modificación estructural reduce significativamente el riesgo de desarrollo de anticuerpos antifármacos (ADA).
Relevancia en la investigación traslacional y preclínica
Los anticuerpos quiméricos se usan ampliamente en ensayos de bloqueo de receptores, estudios de neutralización de citoquinas y modelos de enfermedades in vivo que requieren administración de anticuerpos a largo plazo. Sus regiones constantes parcialmente humanizadas mejoran la compatibilidad con los sistemas de receptores Fc humanos, al tiempo que conservan la afinidad de unión a los antígenos diana validados en la fase de descubrimiento de anticuerpos murinos. Este rendimiento está respaldado por una cartera completa de reactivos de soporte, que incluye más de 18.000 productos de anticuerpos y una amplia gama de reactivos de proteínas e inmunoensayos, lo que permite la validación integrada a través de kits ELISA, sistemas de tinción y sistemas de ensayo bioquímico.
Flujo de trabajo de ingeniería y validación
La producción de anticuerpos quiméricos requiere diseño de construcción génica, construcción vectorial, expresión recombinante en sistemas huésped apropiados, purificación y validación rigurosa de control de calidad (QC), incluyendo determinación del título de anticuerpo basado en ELISA y validación de especificidad de unión.
Un sistema sistemático de gestión de la calidad, que abarca la planificación de la calidad, el monitoreo de la calidad en el proceso, la inspección de la aceptación del producto terminado, el análisis de las causas raíz y la mejora continua, garantiza una excelente consistencia de lote a lote y la preparación para la aprobación regulatoria.
Tipo 3Anticuerpos monoclonales humanizados
Los anticuerpos monoclonales humanizados reducen aún más la inmunogenicidad, ya que solo conservan las regiones determinantes de la complementariedad (CDR) del anticuerpo murino parental. Este formato es de particular importancia para el desarrollo terapéutico que requiere administración a largo plazo y evaluación estricta de la seguridad.
CDR injerto y refinamiento estructural
El injerto de CDR se refiere al trasplante de bucles de CDR de unión a antígenos en una región de marco de inmunoglobulina humana (FR), mientras se conservan residuos clave de marco que soportan la conformación espacial correcta de las CDR.
Se requiere modelado de homología in silico y validación de unión in vitro para evitar la pérdida de afinidad de unión en el marco de anticuerpo humanizado Los ensayos de validación rutinaria incluyen ELISA, transferencia Western, inmunohistoquímica y ensayos funcionales basados en células, que se realizan para confirmar la especificidad de unión retenida y la bioactividad del anticuerpo humanizado.
Abordar la inmunogenicidad y las preocupaciones regulatorias
Los anticuerpos monoclonales humanizados típicamente tienen un contenido de secuencia humana de más del 90%, lo que reduce en gran medida el riesgo de reconocimiento inmune del huésped. La inmunogenicidad reducida mejora la estabilidad in vivo del fármaco, así como la interpretabilidad de los datos de eficacia del fármaco en estudios preclínicos y clínicos.
Para aplicaciones in vivo, el control de endotoxinas requiere típicamente niveles de endotoxinas por debajo de 0,3 UE/mg. La purificación por afinidad mediante cromatografía es un paso crítico en el proceso de producción para satisfacer este requisito.
Integración con plataformas de investigación más amplias
La cartera completa de reactivos de ciencias de la vida de la compañía, que incluye más de 36.000 productos de biología molecular, más de 3.000 productos de biología celular y más de 1.400 kits de ELISA entre especies, proporciona apoyo crítico para experimentos de validación funcional de anticuerpos.
La citación de los anticuerpos monoclonales de la compañía (incluidos los anticuerpos anti-histona H3/HIST3H3 y anti-β-actina) en las principales revistas internacionales demuestra plenamente la fiabilidad de la traducción de sus productos de anticuerpos rigurosamente validados.
Tipo 4Anticuerpos Monoclonales Totalmente Humanos
Los anticuerpos monoclonales totalmente humanos representan el formato de anticuerpo más avanzado en términos de compatibilidad inmune y perfil de seguridad terapéutica. Estos anticuerpos se generan usando tecnologías que incluyen bibliotecas de exhibición de fagos, modelos animales humanizados o secuenciación de células B únicas, todas las cuales producen inmunoglobulinas compuestas enteramente de secuencias humanas.
Tecnologías de generación y estrategias de detección
La visualización de fagos permite la selección in vitro de bibliotecas de anticuerpos altamente diversas y a gran escala. Los modelos animales humanizados que expresan loci de inmunoglobulina humana apoyan el desarrollo in vivo de un repertorio completo de anticuerpos humanos. La clasificación de células B individuales aisla anticuerpos humanos naturales derivados de la respuesta inmune humana. Cada una de estas tecnologías requiere cribado de alto rendimiento y caracterización de afinidad de unión para seleccionar candidatos de anticuerpos óptimos.
Ecosistema de desarrollo de extremo a extremo
El desarrollo exitoso de anticuerpos requiere expresión de antígeno recombinante, síntesis de péptidos para mapeo de epítopos, validación de ensayos bioquímicos y tinción de tejidos enfermos para caracterizar la localización de tejidos del antígeno objetivo. Los servicios de apoyo técnico integrados, incluyendo la síntesis de cebadores, la expresión de proteínas procarióticas, la síntesis de péptidos y el desarrollo de anticuerpos personalizados, forman un flujo de trabajo sin problemas desde el diseño de antígenos hasta la aplicación de inmunoensayos validados.
Análisis comparativo: ¿Cómo seleccionar el tipo de anticuerpo monoclonal apropiado?
La selección de un formato de anticuerpo monoclonal depende de la etapa de investigación, el objetivo terapéutico, la vía de aprobación regulatoria, el presupuesto de costos y el cronograma del proyecto. Los anticuerpos monoclonales murinos son ideales para la investigación básica y el descubrimiento de epítopos; Los anticuerpos quiméricos ofrecen inmunogenicidad reducida para aplicaciones de investigación traslacional; los anticuerpos humanizados proporcionan un perfil de seguridad superior para el desarrollo terapéutico; Los anticuerpos y los anticuerpos totalmente humanos son la elección preferida para aplicaciones que requieren administración a largo plazo e inmunogenicidad mínima.
Beijing Solarbio Ciencia y Tecnología Co., Ltd. complementa estas estrategias con un ecosistema completo de investigación en ciencias de la vida. Sus plataformas de extremo a extremo abarcan la producción de anticuerpos personalizados, incluyendo formatos murinos, quiméricos, humanizados y totalmente humanos, junto con la expresión de proteínas recombinantes, la síntesis de péptidos, kits de ELISA, kits de ensayo bioquímico y reactivos de biología celular. El sistema de gestión de calidad certificado ISO de la compañía garantiza una fiabilidad consistente de lote a lote, alta especificidad y bajos niveles de endotoxinas, apoyando tanto la investigación como el desarrollo terapéutico.
Al integrar cribado de alto rendimiento, tuberías de validación robustas y servicios de personalización flexibles, Solarbio permite a los investigadores agilizar los flujos de trabajo de anticuerpos monoclonales desde el diseño de antígenos hasta la aplicación funcional. Este enfoque integrado no solo acelera los cronogramas experimentales, sino que también mejora la reproducibilidad y la confianza en la traducción, lo que lo convierte en un socio indispensable para los laboratorios que buscan traducir los descubrimientos de anticuerpos en innovaciones clínicas y diagnósticas.
Preguntas frecuentes
Q1: ¿Qué tipo de anticuerpo monoclonal se recomienda para la validación de antígenos en etapa temprana?
R: Los anticuerpos monoclonales murinos son la opción más recomendada para la validación de antígenos en etapa temprana. Esto se debe a que la tecnología del hibridoma permite una alta especificidad de unión y genera líneas celulares monoclonales estables que son compatibles con ensayos de rutina, incluyendo transferencia Western, ELISA e inmunohistoquímica.
Q2: ¿Cómo se puede reducir la inmunogenicidad durante el desarrollo de anticuerpos terapéuticos?
R: La inmunogenicidad puede reducirse significativamente cambiando del formato murino a los formatos de anticuerpos monoclonales quiméricos, humanizados o totalmente humanos. Estos formatos aumentan incrementalmente la proporción de secuencia humana en el anticuerpo, reduciendo el riesgo de desarrollo de anticuerpos antifármacos (ADA).
Q3: ¿Cuál es la línea de tiempo típica para la producción de anticuerpos monoclonales de ratón personalizados?
R: El desarrollo de anticuerpos monoclonales de ratón personalizado típicamente incluye inmunización animal, detección de título de anticuerpos en suero, fusión celular, subclonación y purificación de anticuerpos, y típicamente toma varios meses, dependiendo del rendimiento de cribado y los requisitos de validación.
Q4: ¿Qué cantidad de antígeno se requiere generalmente para la inmunización del ratón?
R: Normalmente, 300-500 μg de antígeno purificado es suficiente para la inmunización de 5 ratones BALB/c en proyectos de desarrollo de anticuerpos monoclonales personalizados.
P5: ¿Se puede integrar el desarrollo de anticuerpos monoclonales con otros ensayos de investigación?
R: Sí, el desarrollo de anticuerpos monoclonales se puede integrar perfectamente con tecnologías de apoyo, incluyendo la expresión de proteínas recombinantes, kits de ELISA, kits de ensayo bioquímico y sistemas de tinción patológica, formando un flujo de trabajo de validación completo que abarca aplicaciones de biología molecular, biología celular e inmunología.