Factores de crecimiento
Clasificación y características
-
Factor de crecimiento derivado de plaquetas (PDGF)
El PDGF se compone de dos subunidades, denominadas cadena A (18 kDa) y cadena B (12-14 kDa), que comparten secuencias peptídicas altamente homólogas, incluyendo 8 residuos de cisteína conservados en posiciones idénticas. PDGF existe en 3 isoformas: los homodímeros PDGF-AA y PDGF-BB, y el heterodímero PDGF-AB. Estas isoformas se distribuyen a través de diversos tejidos y líneas celulares, lo que sugiere funciones biológicas distintas para cada uno.
2 Tipos de receptores de PDGF están presentes en la superficie celular: PDGFR-α y PDGFR-β. PDGFR-α puede unirse tanto a las subunidades A como B de PDGF, mientras que PDGFR-β se une solo a la subunidad B. PDGF-AA se une a dímeros del receptor α, PDGF-AB puede formar dímeros α y β, y PDGF-BB puede activar dímeros del receptor α, β y β. Estos dímeros receptores representan las formas de señalización activas de PDGFR [1].
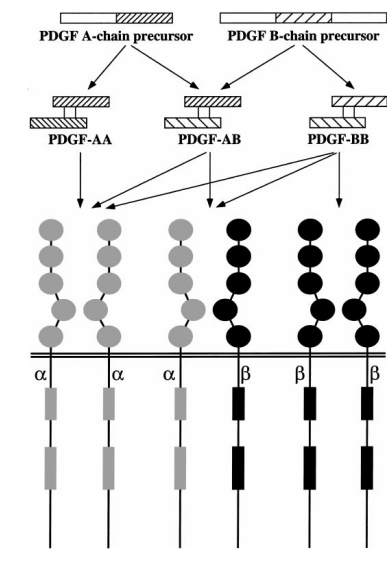
Figura 1: Procesamiento y funciones de isoformas de factor de crecimiento derivado de plaquetas (PDGF) [2]
-
Factor de crecimiento endotelial vascular (VEGF)
El factor de crecimiento endotelial vascular (VEGF), también conocido como factor de permeabilidad vascular (VPF), es un mitógeno altamente específico para las células endoteliales vasculares. La familia VEGF incluye varios miembros: VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E y Factor de Crecimiento de la Placenta (PlGF). Entre ellos, VEGF-A existe en cuatro isoformas principales - VEGF121, VEGF165, VEGF189 y VEGF206 - producidas a través del empalme alternativo de ARNm.
El VEGF ejerce sus efectos biológicos mediante la unión a tres tipos principales de receptores de tirosina quinasa: VEGFR-1 (Flt-1), VEGFR-2 (Flk-1/KDR) y VEGFR-3 (Flt-4). Cada isoforma de VEGF exhibe diferentes afinidades de unión hacia estos receptores, lo que contribuye a la diversidad de las rutas de señalización mediadas por VEGF [3].
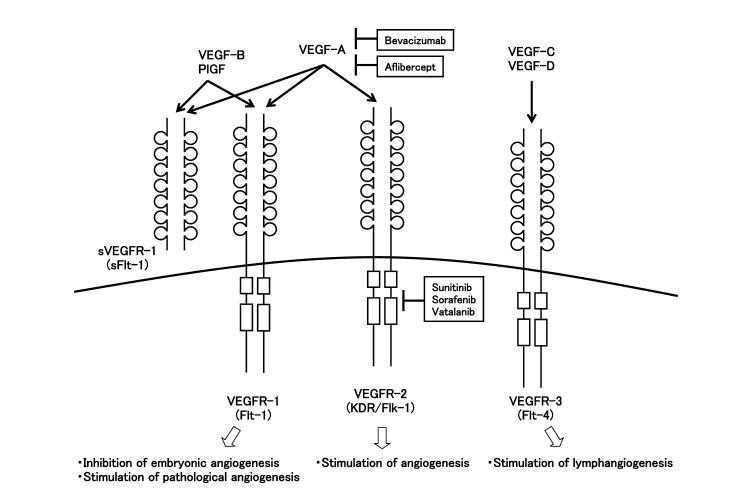
Figura 2: Miembros de la familia VEGF y sus receptores
El VEGF-A se denomina generalmente simplemente VEGF y sirve como un regulador clave de la vasculogénesis del desarrollo, angiogénesis y diferenciación de células progenitoras endoteliales. VEGF-B juega un papel en tumores donde la neovascularización está ausente. VEGF-C y VEGF-D están involucrados en la formación de nuevos vasos sanguíneos y vasos linfáticos dentro de los tejidos tumorales. VEGF-E también se considera un factor angiogénico potencial, mientras que PlGF (Factor de Crecimiento de la Placenta) promueve la neovascularización y aumenta la permeabilidad vascular.
-
Factor de crecimiento epidérmico (EGF)
El factor de crecimiento epidérmico (EGF) es un pequeño polipéptido ampliamente presente en humanos y otros animales, que consiste en una cadena peptídica con 50-60 aminoácidos. Esta cadena contiene 6 residuos de cisteína que forman enlaces disulfuro estables, dando como resultado 3 dominios en bucle críticos para su actividad biológica. Incluso en concentraciones extremadamente bajas, el EGF puede estimular poderosamente el crecimiento celular, inhibir la expresión de genes relacionados con el envejecimiento y retrasar la senescencia celular epidérmica.
El EGF ejerce sus efectos mediante la unión a la región extracelular (que comprende los dominios I-IV) de su receptor, EGFR (Receptor del Factor de Crecimiento Epidérmico), conduciendo a la dimerización de la tirosina quinasa del receptor [4]. Esta activación desencadena una cascada de eventos bioquímicos, incluyendo niveles elevados de calcio intracelular, una mejora de la glicólisis y la síntesis de proteínas, y un aumento de la expresión de ciertos genes, entre ellos el propio gen EGFR. En última instancia, estos eventos promueven la síntesis de ADN y la proliferación celular.
-
Factores de crecimiento de fibroblastos (FGFs)
Los Factores de Crecimiento de Fibroblastos (FGF) son una familia de factores de crecimiento polipéptidos presentes en varios tejidos en todo el cuerpo. Existen principalmente en 2 formas estrechamente relacionadas: FGF básico (bFGF) y FGF ácido (aFGF). La familia FGF consiste en 22 ligandos que pueden interactuar con cuatro receptores FGF distintos (FGFR). La vía de señalización de FGF/FGFR gobierna procesos celulares fundamentales tales como supervivencia celular, proliferación, migración, diferenciación, desarrollo embrionario, organogénesis, reparación/regeneración de tejidos y metabolismo [5].
El nombre “ factor de crecimiento de fibroblastos” refleja su potente efecto mitogénico sobre los fibroblastos. Además, los FGF también estimulan la proliferación de células de músculo liso, condrocitos, queratinocitos y pericitos. Debido a su fuerte afinidad por la heparina, los FGF también se conocen como factores de crecimiento de unión a la heparina. Se sintetizan por células endoteliales vasculares y se almacenan dentro de la membrana basal y la matriz extracelular.
-
Factores de crecimiento similares a la insulina (IGF)
La familia del factor de crecimiento similar a la insulina (IGF) comprende 2 polipéptidos de bajo peso molecular (IGF-1 e IGF-2), 2 tipos de receptores específicos (IGF-1R e IGF-2R, también conocidos como receptores de tipo I y tipo II), y 6 proteínas de unión a IGF (IGFBPs). El IGF-1R comparte una similitud estructural con el receptor de insulina (IR), formando una glicoproteína heterotetramérica (α). ₂β₂) Se compone de 2 subunidades α y 2 subunidades β. La subunidad α contiene el dominio de unión al ligando, mientras que la subunidad β posee actividad de tirosina quinasa intrínseca (pero sin actividad de tirosina).
Las afinidades de unión de insulina e IGF a sus respectivos receptores varían:
- Para el receptor de insulina (IR): Insulina > IGF-1 > IGF-2
- Para el receptor IGF-1 (IGF-1R): IGF-1 > IGF-2 > Insulina
- Para el receptor IGF-2 (IGF-2R): IGF-2 > IGF-1, sin reactividad cruzada observada para la insulina.
El IGF-1 es una proteína básica de cadena única compuesta por 70 aminoácidos, con un peso molecular de aproximadamente 7.649 Da y una notable estabilidad térmica. El IGF-2, por otro lado, es una proteína ligeramente ácida de cadena única con 67 aminoácidos y un peso molecular de aproximadamente 7.471 Da, y es estable en SDS al 0,1%. Los 2 comparten más del 70% de homología de secuencia y aproximadamente el 50% de similitud estructural y funcional con la proinsulina humana.
-
Factores de Crecimiento Transformadores (TGFs)
Los factores de crecimiento transformadores (TGFs) se refieren a 2 clases de factores de crecimiento polipéptidos: TGF-α y TGF-β. El TGF-α es producido por macrófagos, células cerebrales y células epidérmicas, y juega un papel en la inducción del desarrollo epitelial.
En humanos, TGF-β existe en tres isoformas: TGF-β1, TGF-β2 y TGF-β3. Estas isoformas se unen a un complejo receptor compartido compuesto por el receptor TGF-β tipo I (TGF-βR1) y tipo II (TGF-βR2), induciendo cascadas de señalización intracelular similares in vitro [6].
TGF-β (Transforming Growth Factor Beta) es una proteína multifuncional que regula una amplia gama de procesos celulares, incluyendo el crecimiento celular, la diferenciación, la apoptosis y la modulación inmune. Los receptores TGF-β son receptores de serina/treonina quinasa, y la señalización aguas abajo es mediada principalmente a través de la vía SMAD y/o la vía DAXX.
-
Factor de crecimiento del tejido conectivo (CTGF)
El factor de crecimiento del tejido conectivo (CTGF), también conocido como FISP12 o CCN2, pertenece a la familia de proteínas CCN, que incluye 3 miembros: Cyr61, CTGF y Nov.
- un dominio de unión al factor de crecimiento similar a la insulina N-terminal (IGFBP),
- una repetición del factor de von Willebrand tipo C (VWC),
- una repetición de trombospondina tipo 1 (TSP1),
- y un dominio C-terminal (CT) rico en cisteína.
El CTGF se identificó por primera vez en 1991 como la proteína secretada inducible por fibroblastos-12 (FISP12), aislada de células NIH3T3 activadas en suero. El nombre “factor de crecimiento del tejido conectivo” fue propuesto más tarde ese mismo año.
El CTGF fue reconocido inicialmente por su capacidad para promover la proliferación de fibroblastos, la migración, la adhesión y la producción de matriz extracelular (ECM). Cada uno de sus dominios estructurales puede unirse a proteínas asociadas específicas, lo que permite al CTGF realizar una amplia gama de funciones biológicas [7] (ver Figura 3).
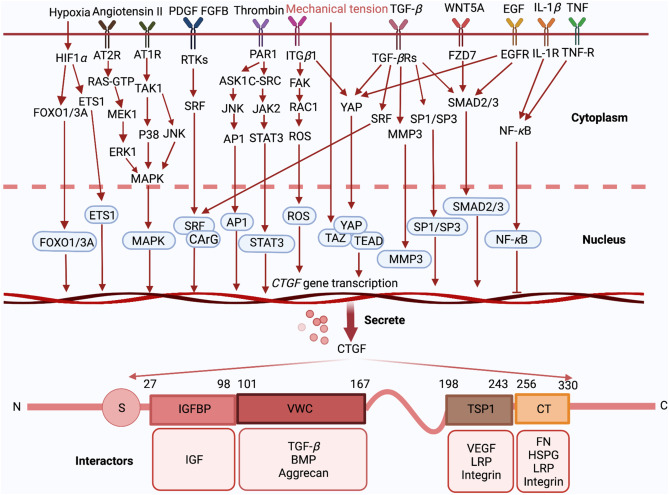
Figura 3
Tras la estimulación externa, se activan las vías de señalización relacionadas con el CTGF, lo que conduce a la transcripción y secreción del CTGF. Después de la secreción, los cuatro dominios distintos de CTGF -IGFBP, VWC, TSP1 y CT- pueden interactuar con varias moléculas para ejercer sus funciones fisiológicas.
-
Factor de crecimiento de queratinocitos (KGF)
El factor de crecimiento de queratinocitos (KGF) es un factor de crecimiento de proteína básico secretado por células mesenquimales en tejidos subcutáneos. Específicamente estimula varios procesos fisiológicos en las células epiteliales, incluyendo el metabolismo, la regeneración, la diferenciación y la migración. KGF es una proteína soluble bioactiva de origen natural en el cuerpo humano, codificada por una secuencia de 194 aminoácidos. La forma madura de KGF consiste en 163 residuos de aminoácidos y contiene un sitio de glicosilación N-terminal.
El KGF se secreta principalmente por el tejido subcutáneo y se une específicamente a su receptor en la superficie de las células epiteliales. A través de una cascada de señalización compleja, activa la expresión de los genes involucrados en la división y el crecimiento celulares, promoviendo así la actividad metabólica y la regeneración de los tejidos epiteliales.
-
Factor de crecimiento nervioso (NGF)
La familia del factor de crecimiento nervioso (NGF) incluye varios factores neurotróficos: el propio NGF, el factor neurotrófico derivado del cerebro (BDNF), la neurotrofina-3 (NT-3), la neurotrofina-4/5 (NT-4/5) y, en menor medida, la neurotrofina-6 y la neurotrofina-7. Entre ellos, los primeros cuatro son los más destacados y bien estudiados.
NGF es el miembro más esencial y representativo de esta familia. En los tejidos, el NGF está presente principalmente en una forma precursora, que se procesa en su forma madura principalmente en la glándula submandibular. El NGF desempeña múltiples papeles, incluyendo apoyar la supervivencia neuronal, proteger los nervios, promover la regeneración nerviosa, modular las respuestas inmunes, facilitar la curación de heridas e inhibir el crecimiento tumoral.
Además de los factores de crecimiento mencionados anteriormente, otros miembros importantes incluyen factores de crecimiento relacionados con la interleucina (tales como IL-1 e IL-3), eritropoyetina (EPO) y factores estimulantes de colonias (CSF). Estas moléculas también desempeñan un papel crítico en la regulación de la proliferación celular, la diferenciación y las respuestas inmunes dentro de varios contextos fisiológicos y patológicos.
Mecanismo de Acción
-
Modos de Acción
Endocrino: Los factores de crecimiento se secretan y transportan a través del torrente sanguíneo para actuar sobre las células objetivo distantes. Un ejemplo es el factor de crecimiento derivado de plaquetas (PDGF).
Los factores de crecimiento secretados por una célula actúan sobre las células cercanas de un tipo diferente, influyendo en su comportamiento.
Los factores de crecimiento actúan en la misma célula que los sintetizó y los secretó.
Entre estos, la señalización paracrina y autocrina son los modos de acción predominantes para la mayoría de los factores de crecimiento.
-
Camino mecánico
Después de ser secretados por varios tipos de células, los factores de crecimiento (GF) ejercen sus efectos biológicos mediante la unión a receptores específicos situados en la superficie o dentro de las células diana. Tras la unión al ligando, estos receptores activan cascadas de señalización intracelular que median las respuestas biológicas correspondientes.
Una clase principal de receptores de factor de crecimiento posee actividad de tirosina quinasa intrínseca y se conoce como tirosina quinasas receptoras (RTK). Las RTK se dividen en aproximadamente 20 familias, incluyendo la familia del receptor del factor de crecimiento epidérmico (EGFR), la familia del receptor del factor de crecimiento derivado de plaquetas (PDGFR) y la familia del receptor del factor de crecimiento nervioso (NGFR). Las acciones de la mayoría de los factores de crecimiento se median a través de RTK (ver Figura 4).
Cuando un factor de crecimiento se une a su receptor en la superficie celular, la transducción de señal se inicia mediante la dimerización de las RTK y la posterior activación de sus dominios de quinasa. Los dos monómeros dentro del dímero RTK se someten a fosforilación cruzada sobre residuos de tirosina, activando completamente el receptor. Estos residuos de tirosina fosforilada en las colas C-terminales de los RTK sirven como sitios de acoplamiento para múltiples moléculas de señalización aguas abajo.
La formación de estos complejos de señal RTK conduce a la activación de varias rutas de señalización aguas abajo, incluyendo las rutas Ras/Erk, PI3K/Akt, Src/Jak/Stat y PLC-γ1. Estas vías interactúan entre sí para formar una red de señalización compleja [8].
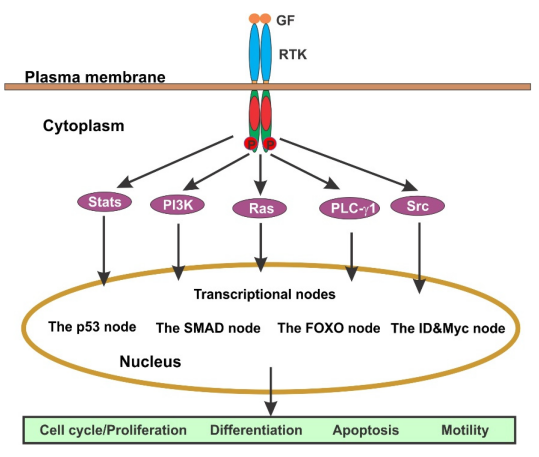
Figura 4
Ruta de señalización RTK-Ras:
Ligando de unión → Activación de la tirosina quinasa receptora (RTK) → RTK activado recluta proteínas adaptadoras → Factor de intercambio de nucleótidos guanina (GEF) promueve la liberación del PIB → Activación de Ras (una proteína de unión a GTP).
Esta activación desencadena una cascada de eventos aguas abajo:
Ras activado inicia la activación de Raf, una proteína quinasa de serina/treonina (también conocida como MAPKKK), que fosforila los residuos de serina/treonina en las proteínas diana. → Raf activado se une a y fosforila MAPKK (MAPK quinasa), conduciendo a su activación. MAPKK es una quinasa de doble especificidad capaz de fosforilar tanto residuos de treonina como tirosina en MAPK, activando así la MAPK. → La MAPK activada se transloca al núcleo → Fosforilación de otras quinasas o proteínas reguladoras génicas (es decir, factores de transcripción), modulación de la expresión génica (véase la Figura 5).
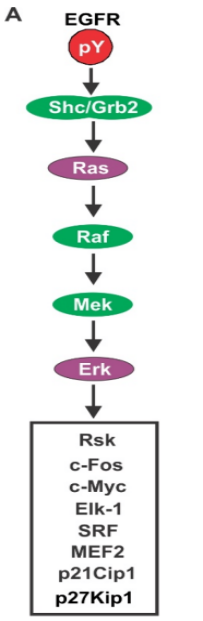
Figura 5
Referencias
1 Kaji K. Función, estructura molecular y regulación de la expresión génica del factor de crecimiento derivado de plaquetas. Nihon Rinsho. agosto de 1992; 50(8):1902-1909.
2 Heldin CH, Westermark B. Mecanismo de acción y papel in vivo del factor de crecimiento derivado de plaquetas. Physiol Rev. 1999 Oct.; 79(4):1283-1316.
Takahashi S. Factor de crecimiento endotelial vascular (VEGF), receptores de VEGF y sus inhibidores para la terapia antiangiogénica del tumor. Biol Farm Bull. 2011; 34(12):1785-1788.
Ogiso H, Ishitani R, Nureki O, et al. Estructura cristalina del complejo de dominios extracelulares del factor de crecimiento epidérmico humano y del receptor. Celular. 2002 Sep 20; 110(6):775-787.
5 Mossahebi-Mohammadi M, Quan M, Zhang JS, et al. Pathway de señalización de FGF: un regulador clave de la pluripotencia de células madre. Desarrollo de células frontales Biol. 2020 Feb 18; 8:79.
6 Sun T, Vander Heiden JA, Gao X, et al. Inhibición de TGF-β3 selectiva por isoforma para la esclerosis sistémica. Med. 2024 9 de febrero; 5(2):132-147.e7.
Fu M, Peng D, Lan T, et al. Factor de crecimiento del tejido conectivo de proteína reguladora multifuncional (CTGF): un objetivo terapéutico potencial para diversas enfermedades. Acta Pharm Sin B. 2022 abril; 12(4):1740-1760.
8 Wang Z. Regulación de la progresión del ciclo celular por señalización celular inducida por factor de crecimiento. Cells 2021, 10, 3327.
Productos relacionados:
Si quieres obtener más detalles, por favor visita nuestro sitio web de la Tienda: www.solarbio.com.
|
Cat No. |
Nombre del producto |
Cat No. |
Nombre del producto |
|
SEKH-0052 |
Kit ELISA VEGF humano |
SEKH-0050 |
Kit ELISA EGF humano |
|
SEKH-0316 |
Kit de ELISA TGF-β1 humano |
SEKM-0035 |
Kit de ELISA TGF-β1 de ratón |
|
SEKM-0039 |
Kit ELISA VEGF de ratón |
SEKR-0032 |
Kit ELISA VEGF de rata |
|
SEKR-0010 |
Kit de ELISA EGF de rata |
SEKR-0012 |
Kit de ELISA TGF-β1 de rata |