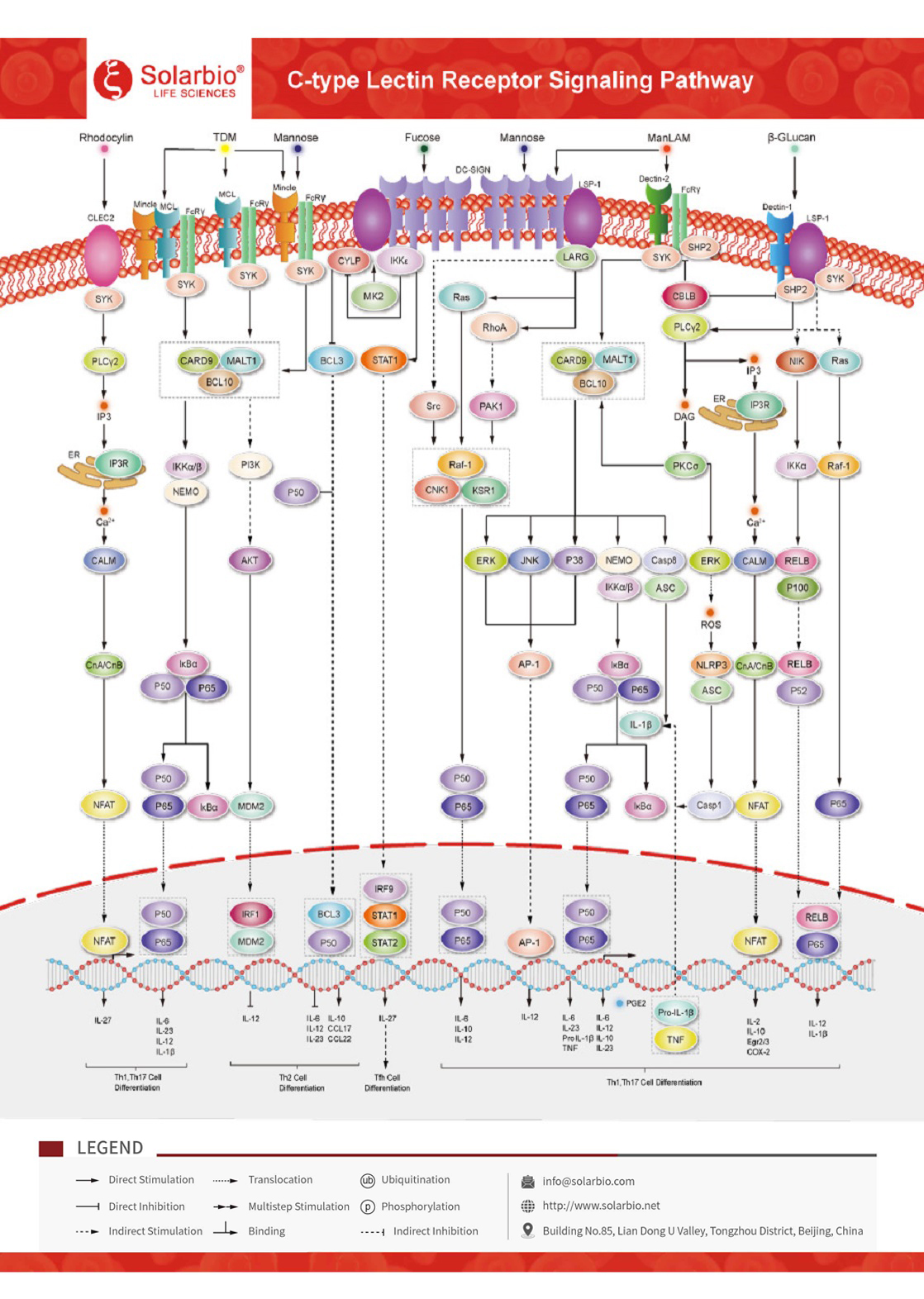
Ruta de señalización del receptor de la lectina de tipo C
Los receptores de lectina de tipo C (CLR), una superfamilia de proteínas que contienen dominio similar a la lectina de tipo C (CTLD), se expresan principalmente en células mieloides. Las CLR de tipo II principales presentes en células dendríticas (DCs) incluyen: molécula de adhesión intercelular específica de DCs 3 que se une a no integrina (DC-SIGN), lectina de tipo C inducible por macrófagos (Mincle), lectina de tipo C asociada a DCS-2 (Dectin-2), antígeno-2 de DCs sanguíneas (BDCA-2), receptor inmune de DCs (DCIR) y receptor de activación inmune de DCs (DC) AR) y así sucesivamente. Después de que el dominio de reconocimiento de azúcar extracelular (CRD) de las lectinas de tipo C se une a los ligandos, el CRD intracelular recluta proteínas aguas abajo a través de la fosforilación y activa la ruta de señalización inmune aguas abajo a través de SYK. SYK puede activar la quinasa IκB (IKK) y múltiples proteínas quinasas activadas por mitógeno (MAPK), incluyendo p38, JNK y ERK1/2, estimulando un complejo multiproteína que consiste en CARD9, Bcl-10 y MALT1 a través de la activación de PKCδ. IKK posteriormente fosforila IκB y promueve la translocación nuclear de NF-κB, mientras que p38, JNK y ERK1/2 fosforilan y activan AP-1. DC-SIGN activa la serina/treonina quinasa Raf-1. La translocación de Raf-1 al núcleo conduce a la fosforilación de la subunidad p65 de NF-κB en serina. Finalmente, p65 se acetila en múltiples sitios de lisina para regular el nivel de transcripción de IL-10. Las CLR estimulan cascadas de señalización intracelular que inducen la producción de citoquinas inflamatorias y quimioquinas, desencadenando así la inmunidad innata y adaptativa a los patógenos.