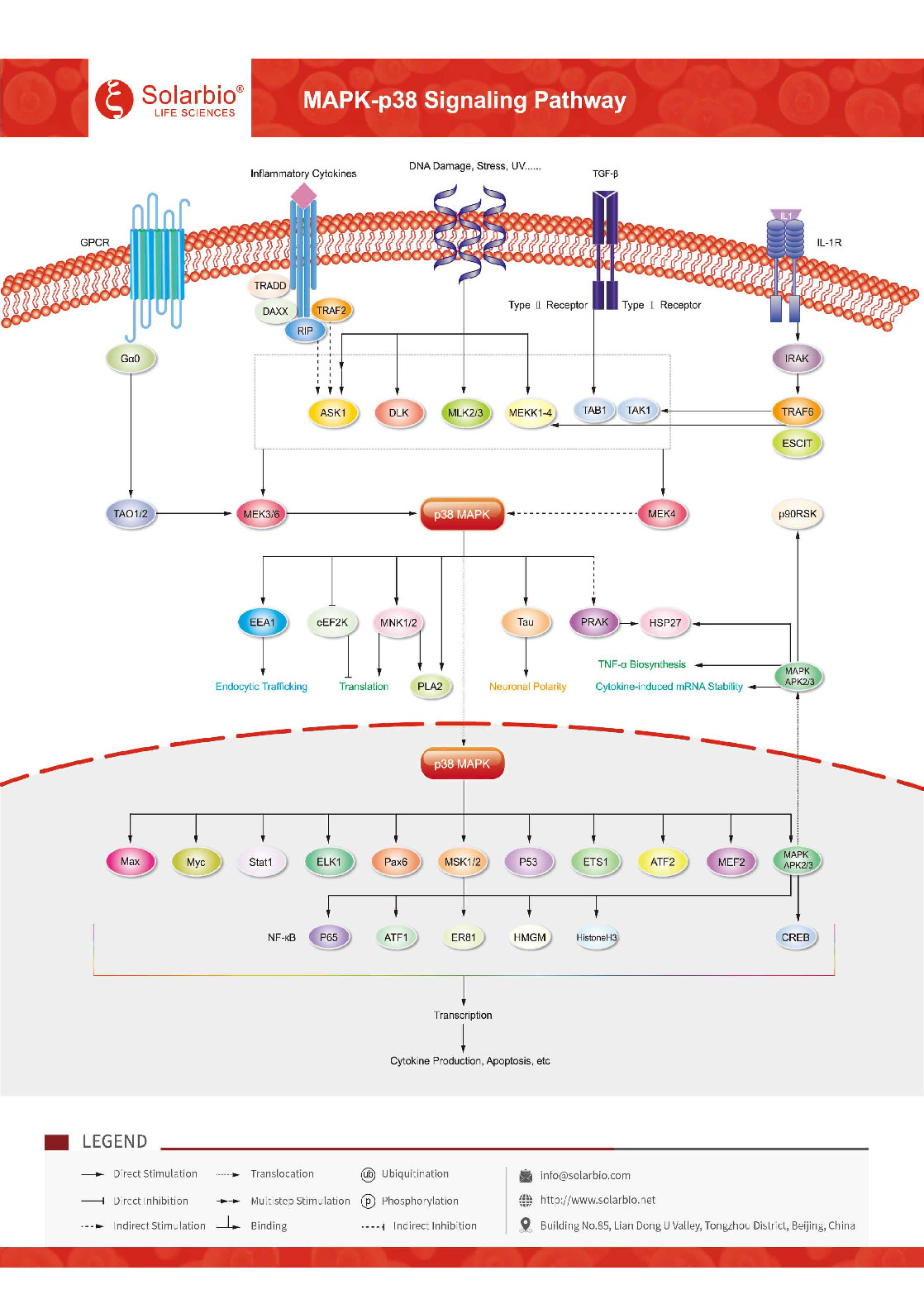
Ruta de señalización MAPK-p38
Las proteinquinasas activadas por mitógeno (MAPK) son una clase de serina/treonina proteinquinasas que están involucradas en una variedad de funciones celulares, incluyendo proliferación celular, diferenciación y migración. La vía de señalización de MAPK está altamente conservada en la evolución celular. Se han encontrado varias vías de señalización de MAPK paralelas en células procarióticas inferiores y células de mamíferos superiores. Diferentes estímulos extracelulares pueden usar diferentes vías de señalización de MAPK para mediar diferentes respuestas biológicas celulares. p38 La MAPK (α, β, γ y δ) es un miembro de la familia MAPK que consiste en proteínas quinasas de serina-treonina dirigidas a prolina altamente conservadas que se activan en respuesta a una variedad de factores de crecimiento, citoquinas y sustancias quimiotácticas (por ejemplo, factor de crecimiento endotelial vascular (VEGF), factor de crecimiento de fibroblastos (FGF)). PDGF, TNF, interleucina, lipopolisacárido (LPS) y formil-metionil-leucil-fenilalanina (fMLP). Es bien conocido que p38 median la inflamación y la apoptosis, convirtiéndose así en un objetivo para el desarrollo de fármacos antiinflamatorios. En la ruta de señalización de MAPK p38, MAPKKK fosforila y activa MKK3/6, que es una quinasa de MAPK p38. MKK3/6 también puede activarse directamente por ASK1 en respuesta a la estimulación de factores apoptóticos. p38 La MAPK está involucrada en la regulación de HSP27, MAPKAPK-2 (MK2), MAPKAPK-3 (MK3) y varios otros factores de transcripción, incluyendo ATF-2, Stat1, complejo Max/Myc, MEF-2 y Elk-1, mientras que CREB se regula indirectamente a través de la activación de MSK1.