¿Qué moléculas biológicas son anticuerpos?
Tabla de Contenidos
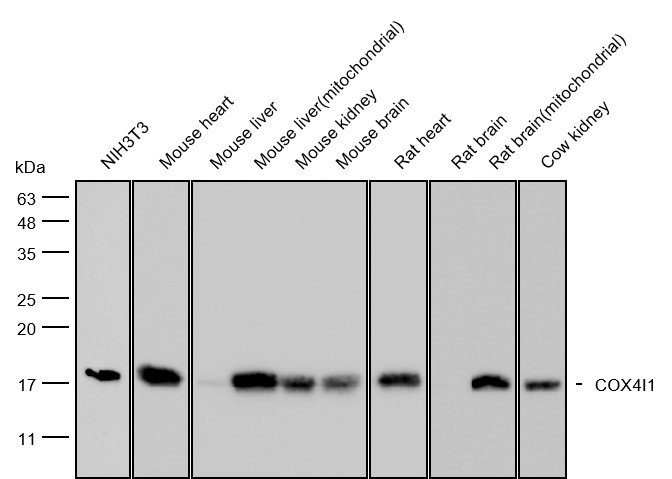
Los anticuerpos, también conocidos como inmunoglobulinas, son glicoproteínas en forma de Y producidas por células plasmáticas y son centrales para la inmunidad adaptativa. Su compleja estructura cuaternaria, combinada con patrones de glicosilación variables, los hace particularmente sensibles a las condiciones de fabricación y manipulación. Para los científicos de banco, esta sensibilidad se traduce en un desafío persistente: lotes de anticuerpos de diferentes proveedores, o incluso del mismo proveedor, pueden producir patrones de transferencia Western inconsistentes, señales ELISA variables, antecedentes no específicos altos en inmunofluorescencia. Si bien una validación rigurosa de la fabricación es esencial, las causas raíz difieren fundamentalmente entre los anticuerpos policlonales (inherentemente variables debido a las respuestas inmunes policlonales) y los anticuerpos monoclonales o recombinantes (donde la variabilidad se deriva más de las condiciones de producción y la deriva genética). Abordar esta crisis de reproducibilidad, por lo tanto, requiere no solo un mejor control de calidad, sino también estándares de validación de anticuerpos que tengan en cuenta estas distinciones biológicas.
Los anticuerpos son glicoproteínas especializadas
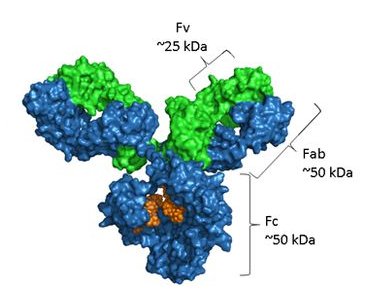
Estructuralmente, los anticuerpos están compuestos por dos cadenas pesadas idénticas y dos cadenas ligeras idénticas, ya sea de isotipo κ o λ, unidas por enlaces disulfuro en una estructura cuaternaria característica en forma de Y. Las regiones Fab (unión a antígeno de fragmento) en los brazos del Y contienen dominios variables (VH y VL) que llevan cada una tres regiones determinantes de complementariedad (CDR) que confieren especificidad de antígeno. La región Fc (cristalizable por fragmento) media en funciones efectoras, tales como la activación del complemento y la unión a receptores Fc en células inmunes, y lleva un sitio de glicosilación unido a N conservado en Asn297 que modula la solubilidad, la estabilidad y la citotoxicidad celular dependiente de anticuerpos (ADCC).
Esta arquitectura de glicoproteínas explica por qué el rendimiento de los anticuerpos es exquisitamente sensible a las condiciones de fabricación. Debido a que la glicosilación de Fc es una modificación postraduccional catalizada por glicosiltransferasas de células huésped, su patrón depende altamente del sistema de expresión (por ejemplo, células CHO, NS0 o HEK293) y de los parámetros de cultivo. Los glicanos Fc de IgG son estructuralmente heterogéneos, y su composición impacta directamente en la función: la ausencia de fucosa del núcleo mejora el ADC a través del compromiso reforzado de FcγRIIIa; la bisección de GlcNAc y alta galactosa (G2) promueven la citotoxicidad dependiente del complemento (CDC); el ácido α2,6-siálico terminal en el glicano Fc se acopla a DC-SIGN para ejercer efectos antiinflamatorios; mientras que las glicoformas agalactosiladas (G0), prevalentes en estados inflamatorios crónicos, muestran CDC reducidos y perfiles efectores Fc alterados. La variación por lotes a menudo surge de una glicosilación inconsistente durante el cultivo celular. En consecuencia, el control de calidad eficaz debe extenderse más allá de los ensayos de concentración de proteínas para incluir el perfilado de glicanos, típicamente mediante HILIC-UPLC o CE-LIF, para garantizar la consistencia funcional en los lotes de fabricación.
Nota: El azul representa la cadena pesada, el verde representa la cadena ligera y la parte naranja es la glicosilación.
Clasificación de anticuerpos: adaptación de propiedades moleculares a las necesidades de investigación
Comprender la clasificación de anticuerpos a nivel molecular permite una selección informada de reactivos:
Por isotipo (Variantes de cadena pesada):
- IgGAnticuerpo sérico predominante (75-80%), estándar para la mayoría de las aplicaciones de investigación; cuatro subclases (IgG1-4) con distintas capacidades de activación del complemento (IgG3 > IgG1 >> IgG2, IgG4), afinidades diferenciales de unión a FcγR y perfiles efectores únicos, en particular IgG4’ Propiedades antiinflamatorias y propensión al intercambio de brazos Fab in vivo
- IgMPredominantemente pentamérica en suero, la primera anticodiclasa producida en las respuestas inmunes primarias; monomérico cuando se expresa como el receptor de células B (BCR) junto con IgD
- IgAExiste como dos subclases (IgA1, IgA2); predominantemente diméricas en secreciones mucosas mediante polimerización mediada por cadena J. IgA2’ La región de bisagra más corta confiere una mayor resistencia a las proteasas bacterianas, lo que la hace particularmente relevante para la investigación del microbioma intestinal.
- IgEMonomérico, central a hipersensibilidad tipo I e inmunidad anti-helminto.
- IgDCo-expresado con IgM en células B naives como parte del BCR; cada vez más reconocido por las funciones secretadas en la homeostasis mucosal y la regulación inmune mediada por basófilos.
Por clonalidad:
- Anticuerpos monoclonales (mAbs)Derivado de un solo clon de células B a través de la tecnología del hibridoma, pero ahora también a través de la clasificación de células B individuales, la exposición de fagos o plataformas animales transgénicas, ofreciendo una especificidad sin igual para epítopos individuales. Ideal para ensayos cuantitativos (por ejemplo, ELISA, citometría de flujo) que requieren resultados consistentes y reproducibles.
- Anticuerpos policlonales (pAbs)Reconocer múltiples epítopos en un antígeno objetivo, proporcionando una amplificación de señal robusta y una mayor probabilidad de detectar antígenos desnaturalizados en los que algunos, pero no todos, los epítopos permanecen intactos. Se prefiere para detectar proteínas nativas en inmunohistoquímica y cuando la amplificación de señales de alta afinidad es crítica.
Por especie huésped & Ingeniería:
La elección de las especies huésped (conejo, ratón, cabra, pollo, lama) determina los patrones de reconocimiento de epítopos, los perfiles de reactividad cruzada y la compatibilidad con aplicaciones aguas abajo. Los anticuerpos recombinantes y humanizados expanden aún más el kit de herramientas para el desarrollo terapéutico y diagnóstico.
Funciones biológicas clave de los anticuerpos
Como efectores inmunes del núcleo, los anticuerpos realizan funciones mediadas por distintos dominios estructurales:
Funciones mediadas por Fab:
- Neutralización: Bloquear la entrada del patógeno en las células huésped o neutralizar la actividad de las toxinas a través de la obstrucción estérica y la competencia del receptor.
- ADCC (Citotoxicidad Celular Dependente de Anticuerpos): Dirige las células NK a lisar las células diana recubiertas de anticuerpos a través del enganche de FcγRIIIa.
- ADCP (fagocitosis celular dependiente de anticuerpos): Mediar la engollación de macrófagos de dianas opsonizadas mediante la activación de FcγR
En la investigación, la alta especificidad y afinidad del sitio de unión al antígeno hacen que los anticuerpos sean herramientas de detección indispensables para la transferencia de Western, ELISA, IHC, IF, citometría de flujo y co-inmunoprecipitación (co-IP). En la terapia, las estrategias de ingeniería de Fc, como la afucosilación para mejorar la ADCC o las mutaciones para silenciar la activación del complemento, se explotan activamente para optimizar los resultados clínicos.
De la biología de células B a la fabricación consistente
In vivo, la diversidad de anticuerpos surge de la recombinación V(D)J y la hipermutación somática, un proceso esencial para la inmunidad adaptativa pero incompatible con las demandas de reproducibilidad de la investigación. Para superar esta heterogeneidad inherente, Solarbio emplea plataformas controladas que abarcan el descubrimiento de anticuerpos a la fabricación:
Tecnología de hibridoma: fusiones de células B inmortalizadas con mieloma para una secreción estable de anticuerpos monoclonales a largo plazo;
Expresión de mamíferos recombinantes: células CHO para perfiles de glicosilación controlados (incluyendo glicoformas modificadas mediante modulación de glicosiltransferasa) y células HEK293 para producción transitoria con glicosilación similar a humana;
Exposición de fagos: maduración de afinidad in vitro y selección de fragmentos de anticuerpos (por ejemplo, scFv, Fab), con conductores posteriormente reformatteados en IgG de longitud completa para la producción recombinante.
Los criterios rigurosos de selección de plomo, que abarcan la identidad definida por la secuencia, la especificidad de unión (validada por líneas celulares de knockout/knockdown), la estabilidad térmica y el rendimiento de expresión, son críticos. Los anticuerpos que fallan en estos puntos de referencia inevitablemente exhiben variabilidad de lote a lote al escalar, comprometiendo la reproducibilidad experimental independientemente de la plataforma de producción empleada.
El punto de dolor de la investigación: variabilidad de lote a lote
Una encuesta realizada en 2023 en 1.000 laboratorios de ciencias de la vida identificó la inconsistencia de los reactivos como una causa principal del fracaso de reproducibilidad en los inmunoensayos. Las manifestaciones incluyen bandas débiles/ausentes de transferencia de Western, alta pérdida de fondo o señal en IHC/IF después de la sustitución del lote, y deriva de la curva estándar de ELISA. Estos fallos se originan de variables de fabricación no controladas - fluctuaciones de cultivo celular, inconsistencias de purificación, heterogeneidad de glicoforma no caracterizada - no simplemente validación insuficiente. Sin validación de múltiples aplicaciones (WB, IHC, IF, citometría de flujo, IP) acoplada con confirmación de especificidad (por ejemplo, validación por eliminación), un anticuerpo optimizado para un ensayo con frecuencia tiene un rendimiento inferior en otro, o exhibe una inconsistencia impredecible de lote a lote.
Marco de validación de anticuerpos Solarbio
Beijing Solarbio Ciencia y Technology Co., Ltd. aborda estos desafíos de reproducibilidad a través de una tubería de validación integrada
- Validación cruzada de múltiples aplicaciones
Cada anticuerpo se somete a pruebas en cinco aplicaciones estándar - WB, IHC, IF, FC e IP - más validación de knockout (KO), emparejada con la proteína diana. contexto biológico.
- Cuantificación de afinidad y especificidad
La fuerza de unión se mide mediante Resonancia de Plasmones de Superficie (SPR). El cribado de reactividad cruzada contra proteínas homólogas asegura que la unión fuera de la diana se minimice.
- Protocolos de consistencia de lote a lote
Cada lote de producción es rastreado a través de evaluaciones IPQC, SPC y AQL. Los anticuerpos se purifican mediante cromatografía de afinidad y se suministran en estabilizadores que contienen glicerol para prevenir daños por congelación-descongelación.
- Rendimiento respaldado por citas
Los reactivos de Solarbio se han citado en más de 150.000 publicaciones indexadas por SCI, incluyendo revistas como Nature Medicine (IF 82.9) y Cell (IF 66.85). Aplicaciones específicas de anticuerpos aparecen en estudios que van desde la señalización de fibroblastos de artritis reumatoide hasta la inhibición de la autofagia en modelos de cáncer, proporcionando a los investigadores evidencia revisada por pares de fiabilidad.
De la investigación a los resultados reproducibles
La clasificación de los anticuerpos como glicoproteínas no es meramente académica, sino que informa directamente cómo estos reactivos deben ser fabricados, validados y almacenados para garantizar la fidelidad experimental. Al combinar la comprensión estructural con sistemas de calidad certificados por ISO y validación de múltiples aplicaciones, los investigadores pueden controlar la variación inherente de lote a lote que socava la fiabilidad de los inmunoensayos.
Preguntas frecuentes
Q1: ¿Qué tipo de biomolécula son los anticuerpos?
R: Glicoproteínas (inmunoglobulinas) compuestas de cadenas polipéptidas pesadas y ligeras emparejadas con glicanos enlazados a N en la región Fc.
Q2: ¿Cómo logran los anticuerpos una alta especificidad?
A: A través de regiones determinantes de complementariedad (CDR) en dominios variables, generadas por recombinación V(D)J e hipermutación somática.
Q3: ¿Qué causa la variación de anticuerpos de lote a lote?
R: Heterogeneidad de glicosilación, agregación/fragmentación y deriva del clon del hibridoma. Rigorosos controles de calidad, incluido el perfilado de glicanos y las pruebas de lotes funcionales, para esta variabilidad.
Q4: ¿Se pueden personalizar los anticuerpos para objetivos nuevos o difíciles?
R: Sí. A través de la tecnología del hibridoma, la expresión recombinante y la exposición de fagos, los investigadores pueden generar anticuerpos contra dianas pobremente inmunogénicas, (por ejemplo, moléculas pequeñas, PTM), modificaciones post-traduccionales o epítopos específicos de conformación.
Q5¿Son los anticuerpos Solarbio adecuados para uso clínico?
R: No. Solo para uso de investigación (RUO). Los anticuerpos de investigación se fabrican sin cumplimiento de GMP, límites de endotoxinas validados o expedientes regulatorios necesarios para aplicaciones diagnósticas o terapéuticas.
|
Gato |
Nombre del producto |
Título de la literatura |
Si |
|
K107441P |
Anticuerpo policlonal anti-MYH11 |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K008899P |
Anticuerpo policlonal anti-MYH11 |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K106603P |
Anticuerpo policlonal anti-PDIA3 |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K007444P |
Anticuerpo policlonal anti-DCN |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K002913P |
Anticuerpo policlonal anti-DCN |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K002098P |
Anticuerpo policlonal anti-PDIA3 |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K002095P |
Anticuerpo policlonal anti-MYH11 |
Proteómica espacialmente resuelta de alta resolución de tejidos complejos basada en microfluidica y aprendizaje de transferencia |
45.5 |
|
K200059M |
Anticuerpo monoclonal anti-β-tubulina |
Glibenclamida se dirige a MDH2 para aliviar fenotipos de envejecimiento a través de la modificación epigenética regulada por el metabolismo |
40.8 |
|
K109422P |
Anticuerpo policlonal anti-SLP-76 |
Ingeniería de un interruptor controlable y reversible para inmunoterapias celulares basadas en CAR a través de un sistema de expansión de código genético |
29.5 |
|
K009635P |
Anticuerpo policlonal anti-β-tubulina |
Dispositivos triboeléctricos implantables, biodegradables e inalámbricos para la terapia del cáncer a través de la disrupción de la dinámica de los microtúbulos y las actinas |
29.4 |
|
K009499P |
Anticuerpo policlonal anti-β-tubulina |
Dispositivos triboeléctricos implantables, biodegradables e inalámbricos para la terapia del cáncer a través de la disrupción de la dinámica de los microtúbulos y las actinas |
29.4 |
|
K009362P |
Anticuerpo policlonal anti-β-tubulina |
Dispositivos triboeléctricos implantables, biodegradables e inalámbricos para la terapia del cáncer a través de la disrupción de la dinámica de los microtúbulos y las actinas |
29.4 |
|
K200059M |
Anticuerpo monoclonal anti-β-tubulina |
Dispositivos triboeléctricos implantables, biodegradables e inalámbricos para la terapia del cáncer a través de la disrupción de la dinámica de los microtúbulos y las actinas |
29.4 |
|
K106392P |
Anticuerpo policlonal anti-β-tubulina |
Dispositivos triboeléctricos implantables, biodegradables e inalámbricos para la terapia del cáncer a través de la disrupción de la dinámica de los microtúbulos y las actinas |
29.4 |
|
K008723P |
Anticuerpo policlonal anti-RPL13A |
El direccionamiento intrínseco del ARN huésped por Cas13 limita su utilidad |
28.1 |
|
K006299P |
Anticuerpo policlonal anti-LY6E |
El direccionamiento intrínseco del ARN huésped por Cas13 limita su utilidad |
28.1 |
|
K110275P |
Anticuerpo policlonal anti-PYCR3 |
El direccionamiento intrínseco del ARN huésped por Cas13 limita su utilidad |
28.1 |
|
K006805P |
Anticuerpo policlonal anti-OASL |
El direccionamiento intrínseco del ARN huésped por Cas13 limita su utilidad |
28.1 |
|
K108466P |
Anticuerpo policlonal anti-RBBP4 |
El ácido γ-aminobutírico derivado de neuronas GABAergico entérico inicia la expresión de Igfbp7 para mantener la homeostasis ILC3 |
27.7 |
|
K200015M |
Etiqueta Anti-mCherry Anticuerpo monoclonal |
Los virus de ARN de cadena única de sentido positivo de plantas y animales codifican pequeñas proteínas importantes para la infección viral en su cadena de sentido negativo. |
27.5 |
|
K200057M |
Anticuerpo monoclonal anti-GAPDH |
Simbiosis de un solo paso de nanopartículas de peróxidos bimetálicos para inducir la ferroptosis/cuproptosis y activar la vía cGAS-STING para una inmunoterapia tumoral mejorada |
27.4 |
|
K200058M |
Anticuerpo monoclonal anti-β-actina |
Simbiosis de un solo paso de nanopartículas de peróxidos bimetálicos para inducir la ferroptosis/cuproptosis y activar la vía cGAS-STING para una inmunoterapia tumoral mejorada |
27.4 |
|
K114465P |
Anticuerpo policlonal anti-M6PR |
Una Nanoplataforma de Quimera de Lidosoma Bifuncional para la Degradación de la Proteína Selectiva del Tumor y la Inmunoterapia del Cáncer Mejorada |
27.4 |
|
K009721P |
Anticuerpo policlonal anti-RAGE |
Las quimeras multifuncionales dirigidas a lisosomas activadas por biomarcadores mediaron la degradación selectiva de las fibrillas amiloides extracelulares |
23.5 |
|
K001593P |
Anticuerpo policlonal anti-Bax |
Sistema de estimulación del nervio vago de bajo nivel de circuito cerrado basado en nanogenerador híbrido para el tratamiento de la fibrilación auricular |
20.577 |
|
K001594P |
Anticuerpo policlonal anti-BCL2 |
Sistema de estimulación del nervio vago de bajo nivel de circuito cerrado basado en nanogenerador híbrido para el tratamiento de la fibrilación auricular |
20.577 |