Quelle molécule biologique sont les anticorps?
Table des matières
Les anticorps, également connus sous le nom d'immunoglobulines, sont des glycoprotéines en forme de Y produites par les cellules plasmatiques et centrales à l'immunité adaptative. Leur structure quaternaire complexe, combinée à des schémas de glycosylation variables, les rend particulièrement sensibles aux conditions de fabrication et de manutention. Pour les scientifiques de banc, cette sensibilité se traduit par un défi persistant: des lots d'anticorps de différents fournisseurs - ou même du même fournisseur - peuvent produire des modèles de Western blot incohérents, des signaux ELISA variables, des arrière-plans non spécifiques élevés en immunofluorescence. Bien qu'une validation rigoureuse de la fabrication soit essentielle, les causes profondes diffèrent fondamentalement entre les anticorps polyclonaux (intrinsèquement variables en raison des réponses immunitaires polyclonales) et les anticorps monoclonaux ou recombinants (où la variabilité découle davantage des conditions de production et de la dérive génétique). Pour faire face à cette crise de reproductibilité, il faut donc non seulement un meilleur contrôle de qualité, mais aussi des normes de validation des anticorps qui tiennent compte de ces distinctions biologiques.
Les anticorps sont des glycoprotéines spécialisées
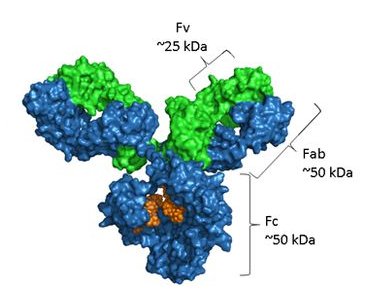
Structurellement, les anticorps sont composés de deux chaînes lourdes identiques et deux chaînes légères identiques - soit κ ou λ isotype - liés par des liaisons disulfures dans une structure quaternaire en forme de Y caractéristique. Les régions Fab (fragment-antigen-binding) aux bras du Y contiennent des domaines variables (VH et VL) portant chacune trois régions déterminantes de complémentarité (CDR) qui confèrent une spécificité antigénique. La région Fc (fragment cristallisable) médie les fonctions effectrices - telles que l'activation du complément et la liaison aux récepteurs Fc sur les cellules immunitaires - et porte un site de glycosylation lié à N conservé à Asn297 qui module la solubilité, la stabilité et la cytotoxicité cellulaire dépendante des anticorps (ADCC).
Cette architecture glycoprotéinienne explique pourquoi les performances des anticorps sont extrêmement sensibles aux conditions de fabrication. Puisque la glycosylation Fc est une modification post-translationnelle catalysée par des glycosyltransférases de cellules hôtes, son schéma dépend fortement du système d'expression (par exemple, cellules CHO, NS0 ou HEK293) et des paramètres de culture. Les glycanes IgG Fc sont structurellement hétérogènes, et leur composition a un impact direct sur la fonction: l'absence de fucose nucléaire améliore l'ADC par un engagement renforcé de FcγRIIIa; la bisection du GlcNAc et du galactose élevé (G2) favorisent la cytotoxicité dépendante du complément (CDC); l'acide α2,6-sialique terminal sur le glycan Fc engage DC-SIGN pour exercer des effets anti-inflammatoires; alors que les glycoformes agalactosylées (G0), prédominantes dans les états inflammatoires chroniques, présentent une CDC réduite et des profils effecteurs Fc altérés. La variation des lots résulte souvent d'une glycosylation incohérente pendant la culture cellulaire. Par conséquent, un contrôle de qualité efficace doit aller au-delà des essais de concentration en protéines pour inclure le profilage de glycane - généralement par HILIC-UPLC ou CE-LIF - pour assurer la cohérence fonctionnelle à travers les lots de fabrication.
Remarque: Le bleu représente la chaîne lourde, le vert représente la chaîne légère et la partie orange est la glycosylation.
Classification des anticorps: correspondance des propriétés moléculaires aux besoins de recherche
Comprendre la classification des anticorps au niveau moléculaire permet une sélection éclairée des réactifs:
Par isotype (variantes de chaîne lourde):
- IgGAnticorps sériques prédominants (75-80%), standard pour la plupart des applications de recherche; quatre sous-classes (IgG1-4) présentant des capacités distinctes d'activation du complément (IgG3 > IgG1 >> IgG2, IgG4), des affinités différentielles de liaison FcγR et des profils effecteurs uniques, notamment IgG4’ Propriétés anti-inflammatoires et propension à l'échange in vivo Fab-bras
- IgMPrédominamment pentamérique dans le sérum, la première anticorpyclasse produite dans les réponses immunitaires primaires; monomère lorsqu'il est exprimé sous forme de récepteur des cellules B (BCR) aux côtés de l'IgD
- IgAIl existe en deux sous-classes (IgA1, IgA2); prédominamment dimérique dans les sécrétions muqueuses par polymérisation médiatée par la chaîne J. IgA2’ La région de charnière plus courte confère une plus grande résistance aux protéases bactériennes, ce qui la rend particulièrement pertinente pour la recherche sur le microbiome intestinal
- IgEMonomère, central à l'hypersensibilité de type I et immunité anti-helminthique.
- IgDCo-exprimé avec IgM sur des cellules B naïves dans le cadre du BCR; de plus en plus reconnue pour ses fonctions sécrétées dans l'homéostase muqueuse et la régulation immunitaire basophile-médiation.
Par clonalité :
- Anticorps monoclonaux (mAbs)Derivé d’un seul clone de cellules B via la technologie de l’hybridome, mais maintenant aussi par le tri de cellules B uniques, l’affichage de phages ou des plateformes animales transgéniques, offrant une spécificité inégalée pour des épitopes simples. Idéal pour les analyses quantitatives (p. ex. ELISA, cytométrie à débit) nécessitant des résultats cohérents et reproductibles.
- Anticorps polyclonaux (pAbs)Reconnaître plusieurs épitopes sur un antigène cible, fournissant une amplification du signal robuste et une probabilité plus élevée de détecter des antigènes dénaturés dans lesquels certains, mais pas tous, les épitopes restent intacts. Préféré pour la détection de protéines natives en immunohistochimie et lorsque l'amplification du signal à haute affinité est critique.
Par espèce hôte & Ingénierie :
Le choix des espèces hôtes (lapin, souris, chèvre, poulet, lama) détermine les schémas de reconnaissance des épitopes, les profils de réactivité croisée et la compatibilité avec les applications en aval. Les anticorps recombinants et humanisés élargissent encore la boîte à outils pour le développement thérapeutique et diagnostic.
Fonctions biologiques clés des anticorps
En tant qu'effecteurs immunitaires de base, les anticorps effectuent des fonctions médiatées par des domaines structurels distincts:
Fonctions médiées par Fab :
- Neutralisation : Bloquer l’entrée des agents pathogènes dans les cellules hôtes ou neutraliser l’activité des toxines par l’entrave stérique et la concurrence des récepteurs.
- ADCC (Cytotoxicité cellulaire dépendante des anticorps): Direction des cellules NK pour lyser les cellules cibles recouvertes d'anticorps via l'engagement FcγRIIIa.
- ADCP (Phagocytose cellulaire dépendante des anticorps): Médier l'engoulement des macrophages de cibles opsonisées par l'activation des FcγR
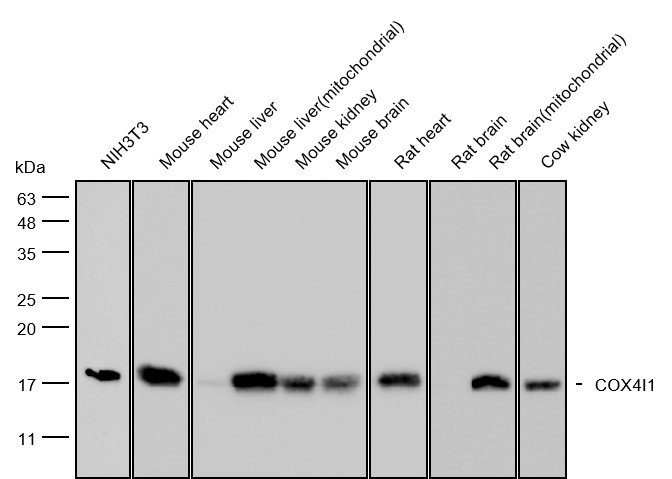
Dans la recherche, la spécificité élevée et l'affinité du site de liaison à l'antigène rendent les anticorps des outils de détection indispensables pour le Western blot, l'ELISA, l'IHC, l'IF, la cytométrie de flux et la co-immunoprecipitation (co-IP). En thérapeutique, les stratégies d'ingénierie Fc - telles que l'afucosylation pour améliorer l'ADCC ou les mutations pour silencier l'activation du complément - sont activement exploitées pour optimiser les résultats cliniques.
De la biologie des cellules B à la fabrication cohérente
In vivo, la diversité des anticorps découle de la recombination V(D)J et de l'hypermutation somatique, processus essentiel à l'immunité adaptative mais incompatible avec les exigences de reproductibilité de la recherche. Pour surmonter cette hétérogénéité inhérente, Solarbio utilise des plateformes contrôlées allant de la découverte des anticorps à la fabrication:
Technologie d’hybridome : fusions immortalisées entre cellules B et myélome pour une sécrétion stable et à long terme d’anticorps monoclonaux ;
Expression recombinante chez les mammifères: cellules CHO pour des profils de glycosylation contrôlés (y compris des glycoformes manipulées via la modulation de la glycosyltransférase) et cellules HEK293 pour une production transitoire avec une glycosylation semblable à celle humaine;
Affichage des phages: maturation d'affinité in vitro et sélection de fragments d'anticorps (p. ex., scFv, Fab), avec des conducteurs reformattés ultérieurement en IgG de longueur complète pour la production recombinante.
Des critères rigoureux de sélection du plomb comprenant l'identité définie par la séquence, la spécificité de liaison (validée par des lignes cellulaires de knockout/knockdown), la stabilité thermique et le rendement d'expression sont essentiels. Les anticorps qui ne remplissent pas ces valeurs de référence présentent inévitablement une variabilité d'un lot à l'autre lors de la mise à l'échelle, compromettant la reproductibilité expérimentale indépendamment de la plateforme de production utilisée.
Le point de douleur de la recherche: la variabilité de lot à lot
Une enquête menée en 2023 dans 1 000 laboratoires de sciences de la vie a identifié l’incohérence des réactifs comme la principale cause de l’échec de la reproductibilité dans les immunoassays. Les manifestations comprennent des bandes de Western blot faibles/absentes, une perte élevée de fond ou de signal dans IHC/IF après le remplacement du lot et la dérive de la courbe standard ELISA. Ces défaillances proviennent de variables de fabrication incontrôlées - fluctuations de culture cellulaire, incohérences de purification, hétérogénéité de glycoforme non caractérisée - et non seulement d'une validation insuffisante. Sans validation multi-application (WB, IHC, IF, cytométrie de flux, IP) couplée à confirmation de spécificité (p. ex., validation par knockout), un anticorps optimisé pour un essai est souvent sous-performant dans un autre, ou présente une incohérence imprévisible de lot à lot.
Cadre de validation des anticorps Solarbio
Pékin Solarbio Science & Technology Co., Ltd. répond à ces défis de reproductibilité grâce à un pipeline de validation intégré
- Validation croisée multi-applications
Chaque anticorps est soumis à des tests dans cinq applications standard - WB, IHC, IF, FC et IP - plus validation par knockout (KO), adaptée à la protéine cible. contexte biologique.
- Quantification de l'affinité et de la spécificité
La force de liaison est mesurée par résonance plasmanique de surface (SPR). Le dépistage de réactivité croisée contre les protéines homologues assure que la liaison hors cible est minimisée.
- Protocoles de cohérence lot à lot
Chaque lot de production est suivi par des évaluations IPQC, SPC et AQL. Les anticorps sont purifiés par chromatographie d'affinité et fournis dans des stabilisateurs contenant du glycérol pour éviter les dommages liés au gel et au dégel.
- Performance soutenue par la citation
Les réactifs Solarbio ont été cités dans plus de 150 000 publications indexées par SCI, y compris des revues telles que Nature Medicine (IF 82.9) et Cell (IF 66.85). Des applications spécifiques d'anticorps apparaissent dans des études allant de la signalisation des fibroblastes de l'arthrite rhumatoïde à l'inhibition de l'autophagie dans des modèles de cancer, fournissant aux chercheurs des preuves de fiabilité évaluées par des pairs.
De la recherche aux résultats reproductibles
La classification des anticorps en tant que glycoprotéines n'est pas seulement académique - elle informe directement comment ces réactifs doivent être fabriqués, validés et stockés pour assurer la fidélité expérimentale. En combinant la compréhension structurelle avec des systèmes de qualité certifiés ISO et la validation multi-applications, les chercheurs peuvent contrôler la variation inhérente de lot à lot qui sape la fiabilité des immunoassays.
FAQ (questions fréquentes)
Q1 : Quel type de biomolécule sont les anticorps ?
R: Glycoprotéines (immunoglobulines) composées de chaînes polypeptidiques lourdes et légères jumelées avec des glycanes liés à N dans la région Fc.
Q2: Comment les anticorps atteignent-ils une spécificité élevée?
R: À travers des régions déterminantes de la complémentarité (CDR) dans des domaines variables, générées par la recombination V(D)J et l'hypermutation somatique.
Q3: Qu'est-ce qui cause la variation d'anticorps d'un lot à l'autre?
R: Hétérogénité de glycosylation, agrégation/fragmentation et dérive du clone d'hybridome. Des contrôles de qualité rigoureux, y compris le profilage des glycanes et les tests fonctionnels des lots, pour cette variabilité.
Q4: Les anticorps peuvent-ils être personnalisés pour des cibles nouvelles ou difficiles?
R: Oui. Grâce à la technologie d'hybridome, à l'expression recombinante et à l'affichage des phages, les chercheurs peuvent générer des anticorps contre des cibles peu immunogènes (p. ex. petites molécules, PTM), des modifications post-translationnelles ou des épitopes spécifiques à la conformation.
Q5Les anticorps Solarbio conviennent-ils à une utilisation clinique ?
R: Non. À des fins de recherche uniquement (RUO). Les anticorps de recherche sont fabriqués sans conformité aux BPF, limites d'endotoxines validées ou dossiers réglementaires requis pour des applications diagnostiques ou thérapeutiques.
|
chat |
nom du produit |
Titre de la littérature |
IF |
|
K107441P |
Anticorps polyclonal anti-MYH11 |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K008899P |
Anticorps polyclonal anti-MYH11 |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K106603P |
Anticorps polyclonaux anti-PDIA3 |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K007444P |
Anticorps polyclonaux anti-DCN |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K002913P |
Anticorps polyclonaux anti-DCN |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K002098P |
Anticorps polyclonaux anti-PDIA3 |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K002095P |
Anticorps polyclonal anti-MYH11 |
Protéomique spatialement résolue à haute résolution de tissus complexes basée sur la microfluidique et l'apprentissage par transfert |
45.5 |
|
K200059M |
Anticorps monoclonaux anti-β-tubuline |
Glibenclamide cible MDH2 pour soulager les phénotypes de vieillissement par la modification épigénétique régulée par le métabolisme |
40.8 |
|
K109422P |
Anticorps polyclonaux anti-SLP-76 |
Ingénierie d'un interrupteur contrôlable et réversible pour les immunothérapies cellulaires basées sur CAR via un système d'expansion du code génétique |
29.5 |
|
K009635P |
Anticorps polyclonal anti-β-tubuline |
Dispositifs triboélectriques implantables, biodégradables et sans fil pour la thérapie du cancer en perturbant la dynamique des microtubules et des actines |
29.4 |
|
K009499P |
Anticorps polyclonal anti-β-tubuline |
Dispositifs triboélectriques implantables, biodégradables et sans fil pour la thérapie du cancer en perturbant la dynamique des microtubules et des actines |
29.4 |
|
K009362P |
Anticorps polyclonal anti-β-tubuline |
Dispositifs triboélectriques implantables, biodégradables et sans fil pour la thérapie du cancer en perturbant la dynamique des microtubules et des actines |
29.4 |
|
K200059M |
Anticorps monoclonaux anti-β-tubuline |
Dispositifs triboélectriques implantables, biodégradables et sans fil pour la thérapie du cancer en perturbant la dynamique des microtubules et des actines |
29.4 |
|
K106392P |
Anticorps polyclonaux anti-β-tubuline |
Dispositifs triboélectriques implantables, biodégradables et sans fil pour la thérapie du cancer en perturbant la dynamique des microtubules et des actines |
29.4 |
|
K008723P |
Anticorps polyclonal anti-RPL13A |
Le ciblage intrinsèque de l'ARN hôte par Cas13 limite son utilité |
28.1 |
|
K006299P |
Anticorps polyclonal anti-LY6E |
Le ciblage intrinsèque de l'ARN hôte par Cas13 limite son utilité |
28.1 |
|
K110275P |
Anticorps polyclonal anti-PYCR3 |
Le ciblage intrinsèque de l'ARN hôte par Cas13 limite son utilité |
28.1 |
|
K006805P |
Anticorps polyclonaux anti-OASL |
Le ciblage intrinsèque de l'ARN hôte par Cas13 limite son utilité |
28.1 |
|
K108466P |
Anticorps polyclonaux anti-RBBP4 |
L'acide γ-aminobutyrique dérivé de neurone GABAergique entérique initie l'expression d'Igfbp7 pour maintenir l'homéostasie ILC3 |
27.7 |
|
K200015M |
Anti-mCherry tag Anticorps monoclonal |
Les virus d'ARN à chaîne unique à sens positif des plantes et des animaux codent de petites protéines importantes pour l'infection virale dans leur chaîne à sens négatif |
27.5 |
|
K200057M |
Anticorps monoclonaux anti-GAPDH |
Symbiose à une étape des nanoparticules de peroxydes bimétalliques pour induire la ferroptose/cuproptose et activer la voie cGAS-STING pour une immunothérapie tumorale améliorée |
27.4 |
|
K200058M |
Anticorps monoclonaux anti-β-actine |
Symbiose à une étape des nanoparticules de peroxydes bimétalliques pour induire la ferroptose/cuproptose et activer la voie cGAS-STING pour une immunothérapie tumorale améliorée |
27.4 |
|
K114465P |
Anticorps polyclonal anti-M6PR |
Une nanoplate-forme de chimère ciblant le lysosome bifonctionnel pour la dégradation protéinique sélective tumorale et l'immunothérapie du cancer améliorée |
27.4 |
|
K009721P |
Anticorps polyclonaux anti-RAGE |
Les chimères multifonctionnelles ciblant les lysosomes activées par des biomarqueurs médiaient la dégradation sélective des fibrilles amyloïdes extracellulaires |
23.5 |
|
K001593P |
Anticorps polyclonaux anti-Bax |
Système de stimulation du nerf vague à faible niveau autonome en boucle fermée basé sur un nanogénérateur hybride pour le traitement de la fibrillation auriculaire |
20.577 |
|
K001594P |
Anticorps polyclonaux anti-BCL2 |
Système de stimulation du nerf vague à faible niveau autonome en boucle fermée basé sur un nanogénérateur hybride pour le traitement de la fibrillation auriculaire |
20.577 |