โมเลกุลชีววิทยาคืออะไร?
ตารางเนื้อหา
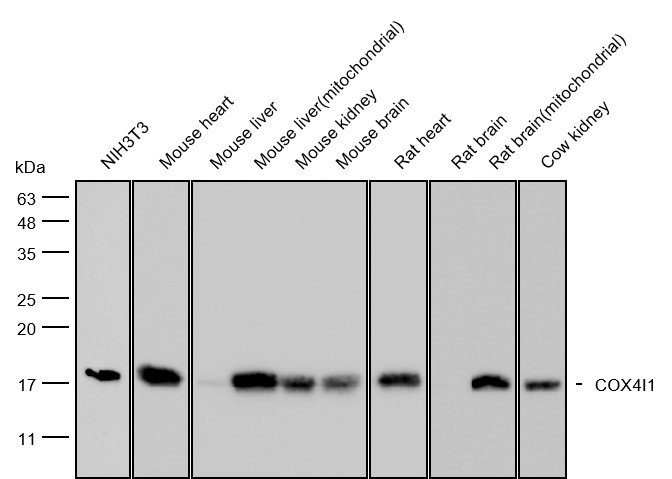
แอนติบอดี - หรือที่รู้จักกันในชื่อ immunoglobulins - ไกลโคโปรตีนรูป Y ที่ผลิตโดยเซลล์พลาสม่าและเป็นกลางของภูมิคุ้มกันที่ปรับตัว โครงสร้างสี่ตัวที่ซับซ้อนของพวกเขา รวมกับรูปแบบ glycosylation ที่แตกต่างกัน ทําให้พวกเขามีความไวโดยเฉพาะต่อสภาพการผลิตและการจัดการ สําหรับนักวิทยาศาสตร์ม้านั่ง ความไวนี้แปลเป็นความท้าทายอย่างต่อเนื่อง: แอนติบอดีจำนวนมากจากซัพพลายเออร์ที่แตกต่างกัน หรือแม้กระทั่งจากผู้ขายเดียวกัน สามารถผลิตรูปแบบ Western blot ที่ไม่สอดคล้อง สั ในขณะที่การตรวจสอบการผลิตอย่างเข้มงวดเป็นสิ่งจำเป็น สาเหตุหลักแตกต่างกันอย่างเป็นพื้นฐานระหว่างแอนติบอดีโพลีคลอน (ที่แปรแปรโดยธรรมชาติเนื่องจากการตอบสนองภูมิคุ้มกันโพลีคลอน) และแอน การแก้ปัญหาวิกฤตการที่สามารถทำซ้ำได้นี้จึงต้องไม่เพียงแค่การควบคุมคุณภาพที่ดีขึ้น แต่ยังต้องมีมาตรฐานการตรวจสอบแอนติบอดี้ท
แอนติบอดีเป็น Glycoproteins พิเศษ
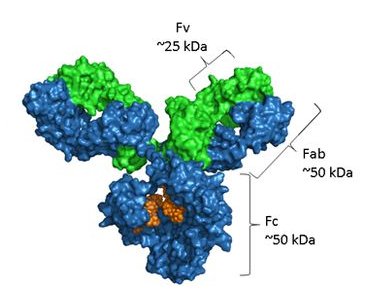
ในโครงสร้าง แอนติบอดีประกอบด้วยสองโซ่หนักที่เหมือนกันและสองโซ่เบาที่เหมือนกัน - ไม่ว่าจะเป็น κ หรือ λ isotype - เชื่อมโยงด้วยพันธุ์ disulfide เป็นโครงสร้างสี่รูปทรง Y ภูมิภาค Fab (Fragment Antigen-binding) ที่แขนของ Y มีโดเมนตัวแปร (VH และ VL) แต่ละภูมิภาคมีสามภูมิภาคที่กําหนดความสมบูรณ์ (CDRs) ที่ให้ความเฉพาะของแอนติเจน ภูมิภาค Fc (ชิ้นส่วนที่สามารถผลึกได้) เป็นกลางฟังก์ชั่น effector เช่นการเปิดใช้งานเสริมและการผูกกับตัวรับ Fc บนเซลล์ภูมิคุ้มกัน และนําสถานที่ glycosylation ที่เกี่ยวข้อง N ที่ Asn297 ที่ปรับความละลาย, ความมั่นคง, และความเป็นพิ
สถาปัตยกรรมไกลโคโปรตีนนี้อธิบายว่าทำไมการทํางานของแอนติบอดี้มีความไวต่อสภาพการผลิตอย่างยอดเยี่ยม เนื่องจาก Fc glycosylation เป็นการปรับปรุงหลังการแปลที่กระตุ้นโดย glycosyltransferases ของเซลล์โฮสต์ รูปแบบของมันขึ้นอยู่กับระบบแสดงออก (เช่น CHO, NS0, หรือเซลล์ HEK293) และพารามิเตอร์การปลูก IgG Fc glycans มีโครงสร้างที่ไม่สม่ำเสมอ และองค์ประกอบของพวกเขามีผลกระทบต่อการทํางานโดยตรง: การไม่มีหลักฟูโคสเพิ่มความร่วมมือ ADCChrough การเสริมสร้าง FcγRIIIa การแบ่ง GlcNAc และ galactose สูง (G2) ส่งเสริมความเป็นพิษในไซต์ที่ขึ้นอยู่กับอุปกรณ์เสริม (CDC); กรดα2,6-sialic บน Fc glycan มีส่วนร่วมกับ DC-SIGN เพื่อให้มีผลต้านการอักเสบ ในขณะที่ agalactosylated (G0) glycoforms ที่แพร่หลายในสภาวะการอักเสบเรื้อรัง แสดง CDC ลดลงและโปรไฟล์ตัวแทน Fc ที่เปลี่ยนแปลง ความแตกต่างของแบทช์มักเกิดขึ้นจากการ glycosylation ที่ไม่สม่ำเสมอในระหว่างการเพาะปลูกเซลล์ ดังนั้นการควบคุมคุณภาพที่มีประสิทธิภาพต้องขยายไปกว่าการทดสอบความเข้มข้นของโปรตีนเพื่อรวมถึงการสร้างโปรไฟล์ของไกลคาน - โดยทั่วไปโดย HILIC-UPLC หรือ CE-LIF - เพื่อให้แน่ใ
หมายเหตุ: สีฟ้าเป็นตัวแทนโซ่หนัก, สีเขียวเป็นตัวแทนโซ่เบา, และส่วนสีส้มเป็น glycosylation.
การจัดประเภทแอนติบอดี้: การจับคู่คุณสมบัติโมเลกุลกับความต้องการในการวิจัย
การเข้าใจการจัดประเภทแอนติบอดีในระดับโมเลกุลทําให้การเลือกสารปฏิกิริยาได้อย่างมีข้อมูล:
ตาม Isotype (ตัวแปรโซ่หนัก):
- IgG: แอนติบอดีเซรั่มที่สำคัญ (75-80%) มาตรฐานสำหรับการใช้งานวิจัยส่วนใหญ่ สี่ชั้นย่อย (IgG1-4) ที่มีความสามารถในการเปิดใช้งานส่วนเสริมที่แตกต่างกัน (IgG3 > IgG1 >> IgG2, IgG4) ความสัมพันธ์ในการผูกพัน FcγR ที่แตกต่างและโปรไฟล์ตัวทำงานที่ไม่ซ้ำกัน คุณสมบัติต่อต้านการอักเสบและแนวโน้มในการแลกเปลี่ยนแขน Fab in vivo
- อิกม: ส่วนใหญ่เป็น pentameric ในเซรั่ม เป็น antibody class แรกที่ผลิตในการตอบสนองภูมิคุ้มกันหลัก โมโนเมอร์เมื่อแสดงเป็นตัวรับเซลล์ B (BCR) พร้อมกับ IgD
- อิกา: มีอยู่เป็นสองคลาสย่อย (IgA1, IgA2); ส่วนใหญ่เป็น dimeric ในการหลั่งเยื่อมผ่าน J-chain-mediated polymerization IgA2’ พื้นที่บานพับสั้นกว่าให้ความต้านทานต่อแบคทีเรียโปรตีเอสมากขึ้น ทําให้มันเป็นที่เกี่ยวข้องโดยเฉพาะสําหรับการวิจัย
- อิกเอ: โมโนเมอร์กลางต่อความไวสูงขึ้นชนิด I และภูมิคุ้มกันต่อเฮลมินท์
- อิกดี: ร่วมแสดงกับ IgM บนเซลล์ B ที่ไม่มีความรู้สึกเป็นส่วนหนึ่งของ BCR ได้รับการยอมรับมากขึ้นสําหรับฟังก์ชั่นที่หลุดใน homeostasis ของเยื่อเมือง และการควบคุมภูมิคุ้มกันที่เป็นกลางโดย basophil
โดย Clonality:
- แอนติบอดี Monoclonal (mAbs): มาจากโคลนเซลล์ B เดียวผ่านเทคโนโลยีไฮบริโดม แต่ตอนนี้ยังผ่านการจัดเรียงเซลล์ B เดียว การแสดงเฟจ หรือแพลตฟอร์มสัตว์ transgenic ที่ให้ความเฉพาะที่ไม่มีเทียบเท่าส เหมาะสำหรับการทดสอบปริมาณ (เช่น ELISA, การวัดไซโตเมตรีการไหล) ที่ต้องการผลลัพธ์ที่สอดคล้องกันและสามารถทำซ้ำได้
- แอนติบอดี Polyclonal (pAbs): รับรู้เอพิโตปหลายตัวบนแอนติเจนเป้าหมาย ให้การขยายสัญญาณที่แข็งแกร่ง และความเป็นไปได้สูงขึ้นในการตรวจจับแอนติเจนที่มีความผิดปกติซึ่งบางอย่าง เหมาะสำหรับการตรวจจับโปรตีนเฉพาะในภูมิคุ้มกัน histochemistry และเมื่อการขยายสัญญาณที่มีความสัมพันธ์สูงเป็นสิ่งสำคัญ
โดยสายพันธุ์ และแอมป์ วิศวกรรม:
การเลือกของสายพันธุ์ที่เป็นเจ้าภาพ (กระต่าย, หนู, แพะ, ไก่, ลาม้) กําหนดรูปแบบการรับรู้เอพิโตป, โปรไฟล์การปฏิกิริยาข้าม, และความเข้ากันได้กับการใช แอนติบอดีที่รวมกันและที่เป็นมนุษย์ยิ่งขยายชุดเครื่องมือสําหรับการพัฒนาการรักษาและการวินิจฉัย
ฟังก์ชั่นชีววิทยาสำคัญของแอนติบอดี
ในฐานะตัวแทนภูมิคุ้มกันหลัก แอนติบอดีทํางานโดยโดเมนโครงสร้างที่แตกต่างกัน:
ฟังก์ชั่น Fab-mediated:
- การเป็นกลาง: ปิดกั้นการเข้าไปในเซลล์โฮสต์ หรือปิดกิจกรรมของสารพิษผ่านอุปสรรคและการแข่งขันตัวรับ
- ADCC (Antibody-Dependent Cellular Cytotoxicity): ตรงเซลล์ NK ไปยังเซลล์เป้าหมายที่เคลือบด้วยแอนติบอดีผ่านการมีส่วนร่วมของ FcγRIIIa
- ADCP (Phagocytosis เซลล์ที่ขึ้นอยู่กับแอนติบอดี้): กลายการกลืนมาโครเฟจของเป้าหมาย opsonized ผ่านการเปิดใช้งาน FcγRs
ในการวิจัยความเฉพาะและความสัมพันธ์สูงของสถานที่ผูกต้องแอนติเจนทำให้แอนติบอดีเป็นเครื่องมือการตรวจจับที่จำเป็นสำหรับ Western blot, ELISA, IHC, IF, flow cytometry และ co-immunoprecipitation (co-IP) ในการรักษากลยุทธ์วิศวกรรม Fc - เช่น afucosylation เพื่อเพิ่ม ADCC หรือการกลายพันเพื่อการเปิดใช้งานเสริมความเงียบ - ถูกใช้อย่างแข็งแกร่งเพื่อปรับปรุงผลลัพธ์ทางคลิน
จากชีววิทยาเซลล์ B ไปยังการผลิตที่สม่ำเสมอ
In vivo ความหลากหลายของแอนติบอดีเกิดขึ้นจากการรวมตัว V(D) J และการเปลี่ยนแปลง somatic hypermutation - กระบวนการที่จําเป็นสําหรับภูมิคุ้มกันที่ปรับตัว แต่ไม่เข้ากันได้กั เพื่อเอาชนะความแตกต่างที่เกิดขึ้นนี้ Solarbio ใช้แพลตฟอร์มที่ควบคุมที่ครอบคลุมการค้นพบแอนติบอดีไปจนถึงการผลิต:
เทคโนโลยีไฮบริโดม: การฟิวชั่นเซลล์ B-myeloma ที่ไม่ตายสําหรับการหลั่งแอนติบอดีโมโนโคลอนระยะยาวที่มั่นคง
การแสดงออกจากสัตว์เลี้ยงลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด้วยลูกด
การแสดงเฟจ: การเป็นผู้ใหญ่ของความสัมพันธ์ใน vitro และการเลือกชิ้นส่วนแอนติบอดี (เช่น scFv, Fab) ด้วยสายนำในภายหลังจากนั้นใหม่รูปแบบเป็น IgG ความยาวเต็มรูปแบบสําหรับการ
เกณฑ์การเลือกตะกั่วที่เข้มงวด - รวมถึงตัวตนที่กําหนดโดยลําดับ, ความเฉพาะของการผูกพัน (ได้รับการตรวจสอบโดยสายเซลล์ knockout / knockdown), ความเสถียรภาพความร้อน, และผล แอนติบอดีที่ล้มเหลวในมาตรฐานเหล่านี้จะแสดงความแตกต่างจากแบทช์ไปยังแบทช์เมื่อขยายขนาด, ทําให้ความสามารถในการทดลองทําซ้ำได้ไม่ว่าจะใช้แพลตฟอร์มการผลิต.
จุดปวดการวิจัย: ความแปรแปรจากแบทช์ไปยังแบทช์
การสํารวจในปี 2023 ทั่วห้องปฏิบัติการวิทยาศาสตร์ชีวิต 1,000 แห่ง ระบุความไม่สอดคล้องกับสารปฏิกิริยาเป็นสาเหตุหลักของความล้มเหลว การปรากฏตัวรวมถึงวง Western blot ที่อ่อนแอ / ไม่มี การสูญเสียพื้นหลังสูงหรือสัญญาณใน IHC / IF หลังจากเปลี่ยนล็อต และการลอยโค้งมาตรฐาน ELISA ความล้มเหลวเหล่านี้เกิดขึ้นจากตัวแปรการผลิตที่ไม่ได้รับการควบคุม - ความผันผวนของการเพาะปลูกเซลล์, ความไม่สอดคล้องการทำความสะอาด, ความไม่สม่ำเสมอของไกลโคฟอร์มที่ไม่มีลักษ โดยไม่มีการยืนยันความเฉพาะ (เช่น การยืนยันความเฉพาะ) แอนติบอดีที่ปรับปรุงสําหรับการทดสอบหนึ่งมักจะมีประสิทธิภาพต่ำกว่าในอีกหนึ่งหรือแสดงความไม่สอดคล้องกันที่ไม่คาดการณ์ได้
โครงการตรวจสอบแอนติบอดี Solarbio
ปักกิ่ง Solarbio Science & บริษัท เทคโนโลยี จํากัด จัดการกับความท้าทายในการทำซ้ำได้เหล่านี้ผ่านท่อการตรวจสอบแบบบูรณาการ
- การตรวจสอบข้ามหลายแอพพลิเคชัน
แอนติบอดีแต่ละตัวได้รับการทดสอบในห้าการใช้งานมาตรฐาน - WB, IHC, IF, FC และ IP - บวกการตรวจสอบ knockout (KO) ที่ตรงกับโปรตีนเป้าหมาย บริบทชีววิทยา
- การวัดปริมาณความสัมพันธ์และความเฉพาะ
ความแข็งแรงของการผูกถูกวัดผ่านการสัมผัสพลาสมอนพื้นผิว (SPR) การตรวจสอบการปฏิกิริยาข้ามกับโปรตีนที่เหมือนกันให้แน่ใจว่าการผูกพันนอกเป้าหมายจะลดลง
- โปรโตคอลความสม่ำเสมอ Lot-to-Lot
การผลิตทุกชุดถูกติดตามผ่านการประเมิน IPQC, SPC และ AQL แอนติบอดีถูกฟอกผ่านโครมาโตกราฟีความเชื่อมโยงและจัดหาในสารเสถียรที่มีกลิเซรอลเพื่อป้องกันความเสียหายจากการแช่แข็งและละละลาย
- การแสดงที่สนับสนุนการอ้างอิง
รีเอเจนต์โซลาร์ไบโอได้รับการอ้างอิงในพิมพ์ที่มีดัชนี SCI มากกว่า 150,000 รายการ รวมถึงวารสารเช่น Nature Medicine (IF 82.9) และ Cell (IF 66.85) การใช้แอนติบอดีเฉพาะเจาะจงปรากฏในการศึกษาตั้งแต่การส่งสัญญาณ fibroblast โรคข้อต่ออักเสบ rheumatoid ไปจนถึงการยับยั้ง autophagy ในรูปแบบมะเร็ง ซึ่งให้นักวิจัยมีหล
จากการวิจัยไปยังผลที่สามารถทำซ้ำได้
การจัดประเภทของแอนติบอดีเป็นไกลิโคโปรตีนไม่ใช่เพียงแค่เรื่องทางวิชาการ มันแจ้งโดยตรงว่า reagents เหล่านี้ต้องผลิต, ตรวจสอบ, และเก็บไว้อย่างไรเพื่อให้แน่ใจว โดยการรวมความเข้าใจโครงสร้างกับระบบคุณภาพที่ได้รับการรับรอง ISO และการยืนยันหลายแอพพลิเคชัน นักวิจัยสามารถควบคุมความแตกต่างของล็อตต่อล็อตที่ทําลายความน่าเชื่
คำถามที่พบบ่อย
Q1: ชีวโมเลกุลชนิดอะไรเป็นแอนติบอดี?
ตอบ: Glycoproteins (immunoglobulins) ประกอบด้วยโซ่โพลีเปปไทด์หนักและเบาที่จับคู่กับ N-linked glycans ในภูมิภาค Fc
Q2: แอนติบอดีบรรลุความเฉพาะสูงได้อย่างไร?
ตอบ: ผ่านภูมิภาคที่กําหนดความสมบูรณ์ (CDRs) ในโดเมนตัวแปร ที่สร้างขึ้นโดยการรวมตัว V(D) J และการเปลี่ยนแปลง somatic hypermutation
Q3: อะไรทําให้เกิดความแตกต่างของแอนติบอดีจากแบทช์ไปยังแบทช์?
ตอบ: ความไม่สม่ำเสมอ glycosylation, การรวม / การแบ่งชิ้นและการเลื่อนไหวของโคลน hybridoma การควบคุมคุณภาพอย่างเข้มงวดรวมถึงการสร้างโปรไฟล์ไกลคานและการทดสอบล็อตที่ใช้งาน การควบคุมความแปรปรานนี้
Q4: แอนติบอดีสามารถปรับแต่งสำหรับเป้าหมายใหม่หรือยากได้หรือไม่?
ตอบ: ใช่ ผ่านเทคโนโลยีไฮบริโดม่า การแสดงออกแบบรวมใหม่ และการแสดงเฟจ นักวิจัยสามารถสร้างแอนติบอดีต่อเป้าหมายที่มีภูมิคุ้มกันที่ไม่ดี (เช่นโมเลกุลเล็ก PTM) การปรับเปลี่ยนหลังการแปลง หร
Q5: แอนติบอดี Solarbio เหมาะสำหรับการใช้งานทางคลินิกหรือไม่?
ตอบ: ไม่ สำหรับการใช้งานวิจัยเท่านั้น (RUO) แอนติบอดีการวิจัยผลิตโดยไม่มีการปฏิบัติตาม GMP, ข้อจำกัด endotoxin ที่ได้รับการยืนยัน, หรือเอกสารกฎหมายที่จําเป็นสําหรับการวินิ
|
แมว |
ชื่อสินค้า |
ชื่อของวรรณกรรม |
ถ้า |
|
K107441P |
แอนติบอดี้ Polyclonal Anti-MYH11 |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K008899P |
แอนติบอดี้ Polyclonal Anti-MYH11 |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K106603P |
แอนติบอดี PDIA3 Polyclonal |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K007444P |
แอนติบอดี Polyclonal Anti-DCN |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K002913P |
แอนติบอดี Polyclonal Anti-DCN |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K002098P |
แอนติบอดี PDIA3 Polyclonal |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K002095P |
แอนติบอดี้ Polyclonal Anti-MYH11 |
โปรตีโอมิกส์ที่มีความละเอียดสูงของเนื้อเยื่อที่ซับซ้อนโดยใช้ microfluidics และการเรียนรู้การโอน |
45.5 |
|
K200059M |
แอนติบอดี้ Monoclonal Anti-β-Tubulin |
Glibenclamide เป้าหมาย MDH2 เพื่อบรรเทา phenotypes ริ้วรอยผ่านการเปลี่ยนแปลง epigenetic ที่ควบคุมโดยการเผาผลาญ |
40.8 |
|
K109422P |
แอนติบอดี SLP-76 Polyclonal |
วิศวกรรมสวิตช์ที่ควบคุมได้และย้อนกลับได้สําหรับการรักษาภูมิคุ้มกันเซลล์ที่ใช้ CAR ผ่านระบบการขยายรหัสพันธุกรรม |
29.5 |
|
K009635P |
แอนติบอดี Anti-β-Tubulin Polyclonal |
อุปกรณ์ Triboelectric ที่สามารถปลูกตัวได้, ย่อยสลายได้ทางชีวภาพและไร้สายสำหรับการรักษามะเร็งผ่านการรบกวนไดนามิกส์ Microtubule และ Actins |
29.4 |
|
K009499P |
แอนติบอดี Anti-β-Tubulin Polyclonal |
อุปกรณ์ Triboelectric ที่สามารถปลูกตัวได้, ย่อยสลายได้ทางชีวภาพและไร้สายสำหรับการรักษามะเร็งผ่านการรบกวนไดนามิกส์ Microtubule และ Actins |
29.4 |
|
K009362P |
แอนติบอดี Polyclonal Anti-β-tubulin |
อุปกรณ์ Triboelectric ที่สามารถปลูกตัวได้, ย่อยสลายได้ทางชีวภาพและไร้สายสำหรับการรักษามะเร็งผ่านการรบกวนไดนามิกส์ Microtubule และ Actins |
29.4 |
|
K200059M |
แอนติบอดี้ Monoclonal Anti-β-Tubulin |
อุปกรณ์ Triboelectric ที่สามารถปลูกตัวได้, ย่อยสลายได้ทางชีวภาพและไร้สายสำหรับการรักษามะเร็งผ่านการรบกวนไดนามิกส์ Microtubule และ Actins |
29.4 |
|
K106392P |
แอนติบอดี Anti-β-Tubulin Polyclonal |
อุปกรณ์ Triboelectric ที่สามารถปลูกตัวได้, ย่อยสลายได้ทางชีวภาพและไร้สายสำหรับการรักษามะเร็งผ่านการรบกวนไดนามิกส์ Microtubule และ Actins |
29.4 |
|
K008723P |
ป้องกัน RPL13A Polyclonal แอนติบอดี |
การตั้งเป้าหมายที่แท้จริงของ RNA โฮสต์โดย Cas13 จํากัดการใช้งานของมัน |
28.1 |
|
K006299P |
แอนติบอดี Polyclonal Anti-LY6E |
การตั้งเป้าหมายที่แท้จริงของ RNA โฮสต์โดย Cas13 จํากัดการใช้งานของมัน |
28.1 |
|
K110275P |
แอนติบอดี Polyclonal Anti-PYCR3 |
การตั้งเป้าหมายที่แท้จริงของ RNA โฮสต์โดย Cas13 จํากัดการใช้งานของมัน |
28.1 |
|
K006805P |
แอนติบอดี Anti-OASL Polyclonal |
การตั้งเป้าหมายที่แท้จริงของ RNA โฮสต์โดย Cas13 จํากัดการใช้งานของมัน |
28.1 |
|
K108466P |
แอนติบอดี Polyclonal Anti-RBBP4 |
GABAergic กรด γ-aminobutyric ที่มาจากเซลล์ประสาทที่เริ่มต้นการแสดงออกของ Igfbp7 เพื่อรักษา ILC3 homeostasis |
27.7 |
|
K200015M |
แท็ก Anti-mCherry แอนติบอดี Monoclonal |
ไวรัส RNA สายเดียวที่มีความรู้สึกบวกของพืชและสัตว์เข้ารหัสโปรตีนเล็ก ๆ ที่สําคัญสําหรับการติดเชื้อไวรัสในสายของพวกเขาที่มีความรู้สึกลบ |
27.5 |
|
K200057M |
แอนติบอดี Monoclonal Anti-GAPDH |
การร่วมชีวิตขั้นตอนเดียวของอนุภาคนาโน Bimetallic Peroxides เพื่อให้เกิด Ferroptosis / Cuproptosis และเปิดใช้งานเส้นทาง cGAS-STING สําหรับการรักษาภูมิคุ้มกันมะเร็งที่เพิ่มขึ้น |
27.4 |
|
K200058M |
แอนติบอดี Anti-β-Actin Monoclonal |
การร่วมชีวิตขั้นตอนเดียวของอนุภาคนาโน Bimetallic Peroxides เพื่อให้เกิด Ferroptosis / Cuproptosis และเปิดใช้งานเส้นทาง cGAS-STING สําหรับการรักษาภูมิคุ้มกันมะเร็งที่เพิ่มขึ้น |
27.4 |
|
K114465P |
แอนติบอดี้ Polyclonal Anti-M6PR |
แพลตฟอร์ม Chimera Nanoplatform ที่เป้าหมาย Lysosome แบบ Bifunctional สําหรับการย่อยสลายโปรตีนเลือกเนื้องอกและการรักษาภูมิคุ้มกันมะเร็งที่เพิ่มขึ้น |
27.4 |
|
K009721P |
แอนติบอดี Polyclonal Anti-RAGE |
Chimeras ที่เป้าหมายลิโซโมมหลายฟังก์ชันที่เปิดใช้งานโดย Biomarker ที่เป็นกลางการย่อยสลายทางเลือกของ extracellular amyloid fibers |
23.5 |
|
K001593P |
แอนติบอดี Anti-Bax Polyclonal |
ระบบการกระตุ้นเส้นประสาทระดับต่ำแบบปิดวงจรแบบไฮบริด nanogenerator สําหรับการรักษา atrial fibrillation |
20.577 |
|
K001594P |
แอนติบอดี Anti-BCL2 Polyclonal |
ระบบการกระตุ้นเส้นประสาทระดับต่ำแบบปิดวงจรแบบไฮบริด nanogenerator สําหรับการรักษา atrial fibrillation |
20.577 |