4 types d'anticorps monoclonaux
Table des matières
Les anticorps monoclonaux servent d'outils critiques en immunologie, en biologie moléculaire, en biologie cellulaire et en médecine translationnelle. Leur regroupement structurel joue un rôle direct dans la fiabilité des tests, le risque de réaction immunitaire, la facilité d'approbation et les possibilités de traitement ultérieur. Lors du choix d'un style d'anticorps monoclonaux, les scientifiques doivent vérifier la précision des antigènes, les nombres de force de liaison, les moyens de détection des épitopes, la réaction croisée et la réponse immunitaire de l'hôte. Ils doivent également penser à établir des calendriers et des configurations de contrôle de qualité qui guident les résultats répétés. Pékin Solarbio Science & Technologie Co., Ltd. a travaillé dans le domaine des réactifs des sciences de la vie depuis 2004. Elle agit en tant qu'entreprise nationale de haute technologie intégrant la R& D, production, vente et service. La société a mis en place une plateforme complète qui couvre les anticorps, les protéines recombinantes, les kits ELISA, les kits d'essais biochimiques, les solutions de coloration, les normes analytiques, les peptides et les composés de petites molécules. La société détient ISO 9001, ISO 13485Certifications ISO 14001 et ISO 45001. Elle a soutenu près de 150 000 publications majeures, dont des articles dans des revues telles que NATURE MEDICINE, CELL et CELL RESEARCH. Cela montre la croissance technique et la qualité de répétition de ses produits immunitaires.
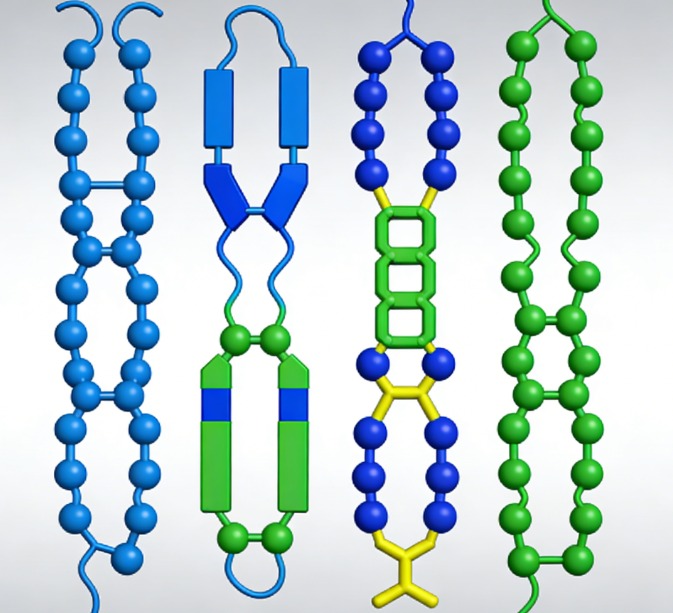
Type 1Anticorps monoclonaux murins
Les anticorps monoclonaux murins sont le premier format d'anticorps dérivés d'hybridome. Ils sont encore largement utilisés dans la recherche de base et la validation des antigènes au stade précoce, en raison de leur spécificité élevée et de leurs protocoles de production matures.
Caractéristiques des anticorps monoclonaux murins
Anticorps monoclonaux murins par immunisation de souris BALB/c avec des antigènes protéiniques purifiés ou peptidiques synthétiques. Ensuite, ils ont récolté des souris immunisées et fusionné avec des cellules de myélome (par exemple, SP2 / 0) à un rapport défini, pour générer des lignées cellulaires d'hybridome stables qui sécrétent des molécules d'immunoglobuline homogènes. Ces anticorps contiennent des régions variables murines complètes (Fv) et des régions constantes (Fc), qui confèrent une grande affinité de liaison aux épitopes cibles, y compris les épitopes linéaires et conformationnels, à condition que des adjuvants appropriés soient utilisés pour maintenir la conformation spatiale native de l'antigène.
Les laboratoires évaluent généralement les titres d'anticorps sériques par ELISA à base de protéines avant la fusion cellulaire. Les lignées d'hybridome positives sont soumises à plusieurs cycles de sous-clonage pour obtenir des lignées cellulaires monoclonales stables, suivies de la production de surnageant de culture et de la purification de l'affinité des anticorps.
Applications et limitations techniques
Les anticorps monoclonaux murins conviennent bien pour la Western blot (WB), l'immunohistochimie (IHC), la coloration par immunofluorescence (IF), la quantification par ELISA et la cartographie des épitopes dans la recherche à un stade précoce. Cependant, la structure immunoglobuline murine complète peut induire une forte réponse d'anticorps anti-souris humains (HAMA).
Développement structuré grâce à des services d'anticorps personnalisés
La plateforme de service d'anticorps personnalisés fournit des services de développement d'anticorps monoclonaux personnalisés de bout en bout de souris, y compris l'immunisation de souris BALB/c, la détection du titre d'anticorps sériques à base d'ELISA, la fusion de splénocytes, le dépistage par surnageant, le sous-clonage, l'établissement d'une lignée cellulaire monoclonale stable et la purification des anticorps.
La préparation rapide de l'antisérum peut être terminée en 3-4 semaines pour les applications où seul l'antisérum polyclonal est nécessaire. Le développement complet d'anticorps monoclonaux prend généralement plusieurs mois, en fonction du débit de dépistage et des exigences de validation. Le dosage d'antigène requis est relativement faible: généralement, 300-500 μg d'antigène purifié est suffisant pour l'immunisation de 5 souris BALB/c, ce qui réduit considérablement la consommation de précieuses protéines recombinantes et de peptides synthétiques.
Type 2Anticorps monoclonaux chimériques
Lorsque la réaction immunitaire devient une préoccupation dans la recherche translationnelle, les anticorps monoclonaux chimériques fournissent un format structurel intermédiaire qui équilibre une spécificité de liaison antigénique élevée avec un risque d'immunogénicité réduit.
Les anticorps monoclonaux chimériques conservent les régions variables murines responsables de la reconnaissance des antigènes, tout en remplaçant les régions constantes murines par des régions constantes de l'immunoglobuline humaine. Cette conception augmente la proportion globale de séquence humaine dans l'anticorps, réduisant ainsi significativement l'immunogénicité.
Conception structurelle et considérations immunologiques
La liaison antigénique est située dans les régions de chaîne variable lourde (VH) et variable légère (VL). La rétention de ces régions préserve entièrement la spécificité épitopique, tandis que le remplacement des régions constantes par des séquences dérivées de l'homme module les fonctions d'effecteur immunitaire médiées par Fc et les caractéristiques de demi-vie sérique de l'anticorps. Par rapport aux immunoglobulines murines complètes, cette modification structurelle réduit considérablement le risque de développement d’anticorps anti-médicaments (ADA).
Pertinence dans la recherche translationnelle et préclinique
Les anticorps chimériques sont largement utilisés dans les essais de blocage des récepteurs, les études de neutralisation des cytokines et les modèles de maladie in vivo qui nécessitent une administration à long terme d'anticorps. Leurs régions constantes partiellement humanisées améliorent la compatibilité avec les systèmes de récepteurs Fc humains, tout en conservant l'affinité de liaison aux antigènes cibles validés dans la phase de découverte d'anticorps murins. Cette performance est en outre soutenue par un portefeuille complet de réactifs de soutien, comprenant plus de 18 000 produits anticorps et une vaste gamme de réactifs de protéines et d'immunoassay, permettant une validation intégrée via des kits ELISA, des systèmes de coloration et des systèmes d'essais biochimiques.
Flow de travail d'ingénierie et de validation
La production d'anticorps chimériques nécessite la conception de constructions géniques, la construction de vecteurs, l'expression recombinante dans des systèmes hôtes appropriés, la purification et la validation rigoureuse du contrôle de qualité (QC), y compris la détermination du titre d'anticorps par ELISA et la validation de la spécificité de liaison.
Un système de gestion de la qualité systématique, couvrant la planification de la qualité, le suivi de la qualité en cours de processus, l'inspection de l'acceptation du produit fini, l'analyse des causes profondes et l'amélioration continue, assure une excellente cohérence de lot à lot et la préparation à l'approbation réglementaire.
Type 3Anticorps monoclonaux humanisés
Les anticorps monoclonaux humanisés réduisent encore l'immunogénicité, car ils ne conservent que les régions déterminantes de la complémentarité (CDR) de l'anticorps murin parental. Ce format est particulièrement important pour le développement thérapeutique nécessitant une administration à long terme et une évaluation rigoureuse de la sécurité.
CDR Greffe et raffinage structurel
La greffe de CDR se réfère à la transplantation de boucles de CDR liant des antigènes dans une région cadre de l'immunoglobuline humaine (FR), tout en conservant des résidus de cadre clés qui soutiennent la conformation spatiale correcte des CDR.
La modélisation de l'homologie in silico et la validation de la liaison in vitro sont nécessaires pour éviter la perte d'affinité de liaison dans le cadre de l'anticorps humanisé. Les essais de validation de routine comprennent l'ELISA, le Western blotting, l'immunohistochimie et les essais fonctionnels à base de cellules, qui sont effectués pour confirmer la spécificité de liaison et la bioactivité retenues de l'anticorps humanisé.
Répondre aux préoccupations en matière d'immunogénicité et de réglementation
Les anticorps monoclonaux humanisés ont généralement une teneur en séquence humaine supérieure à 90%, ce qui réduit considérablement le risque de reconnaissance immunitaire de l'hôte. L'immunogénicité réduite améliore la stabilité in vivo du médicament, ainsi que l'interprétabilité des données d'efficacité du médicament dans les études précliniques et cliniques.
Pour les applications in vivo, le contrôle des endotoxines nécessite généralement des niveaux d'endotoxines inférieurs à 0,3 UE/mg. La purification par affinité par chromatographie est une étape critique dans le processus de production pour répondre à cette exigence.
Intégration avec des plateformes de recherche plus vastes
Le portefeuille complet de réactifs en sciences de la vie de la société, comprenant plus de 36 000 produits de biologie moléculaire, plus de 3 000 produits de biologie cellulaire et plus de 1 400 kits ELISA cross-species, fournit un soutien essentiel pour les expériences de validation fonctionnelle des anticorps.
La citation des anticorps monoclonaux de la société (y compris les anticorps anti-histone H3/HIST3H3 et anti-β-actine) dans les principales revues internationales démontre pleinement la fiabilité translationnelle de ses produits d’anticorps rigoureusement validés.
Type 4Anticorps monoclonaux entièrement humains
Les anticorps monoclonaux entièrement humains représentent le format anticorps le plus avancé en termes de compatibilité immunitaire et de profil de sécurité thérapeutique. Ces anticorps sont générés en utilisant des technologies telles que des bibliothèques d'affichage de phages, des modèles animaux humanisés ou le séquençage de cellules B simples, qui produisent toutes des immunoglobulines composées entièrement de séquences humaines.
Technologies de génération et stratégies de dépistage
L'affichage des phages permet la sélection in vitro à partir de bibliothèques d'anticorps très diverses et à grande échelle. Les modèles animaux humanisés exprimant des loci d'immunoglobuline humaine soutiennent le développement in vivo d'un répertoire complet d'anticorps humains. Le tri des cellules B isole des anticorps humains naturels dérivés de la réponse immunitaire humaine. Chacune de ces technologies nécessite un dépistage à haut débit et une caractérisation d'affinité de liaison pour sélectionner des candidats anticorps optimaux.
Écosystème de développement de bout en bout
Le développement d'anticorps réussi nécessite l'expression d'antigènes recombinants, la synthèse peptidique pour la cartographie des épitopes, la validation d'essais biochimiques et la coloration des tissus malades pour caractériser la localisation tissulaire de l'antigène cible. Les services de soutien technique intégrés, y compris la synthèse d'amorçage, l'expression de protéines prokaryotes, la synthèse de peptides et le développement d'anticorps personnalisés, forment un flux de travail transparent, de la conception des antigènes à l'application d'immunoassay validée.
Analyse comparative: Comment choisir le type d'anticorps monoclonaux approprié?
Le choix d'un format d'anticorps monoclonaux dépend de l'étape de la recherche, de l'objectif thérapeutique, de la voie d'approbation réglementaire, du budget des coûts et du calendrier du projet. Les anticorps monoclonaux murins sont idéaux pour la recherche de base et la découverte d'épitopes; les anticorps chimères offrent une immunogénicité réduite pour les applications de recherche translationnelle; les anticorps humanisés offrent un profil de sécurité plus élevé pour le développement thérapeutique; et les anticorps entièrement humains sont le choix préféré pour les applications nécessitant une administration à long terme et une immunogénicité minimale.
Pékin Solarbio Science & Technologie Co., Ltd. complète ces stratégies avec un écosystème complet de recherche en sciences de la vie. Ses plateformes de bout en bout englobent la production d'anticorps sur mesure, y compris les formats murin, chimérique, humanisé et entièrement humain, ainsi que l'expression protéique recombinante, la synthèse peptidique, les kits ELISA, les kits d'essais biochimiques et les réactifs de biologie cellulaire. Le système de gestion de la qualité certifié ISO de l’entreprise assure une fiabilité cohérente de lot à lot, une spécificité élevée et des niveaux d’endotoxines bas, soutenant à la fois la recherche et le développement thérapeutique.
En intégrant un dépistage à haut débit, des pipelines de validation robustes et des services de personnalisation flexibles, Solarbio permet aux chercheurs de rationaliser les flux de travail des anticorps monoclonaux, de la conception des antigènes à l'application fonctionnelle. Cette approche intégrée accélère non seulement les calendriers expérimentaux, mais améliore également la reproductibilité et la confiance translationnelle, ce qui en fait un partenaire indispensable pour les laboratoires qui visent à traduire les découvertes d’anticorps en innovations cliniques et diagnostiques.
FAQ (questions fréquentes)
Q1: Quel type d'anticorps monoclonaux est recommandé pour la validation des antigènes au stade précoce?
R: Les anticorps monoclonaux murins sont le choix le plus recommandé pour la validation des antigènes au stade précoce. C'est parce que la technologie de l'hybridome permet une spécificité de liaison élevée et génère des lignées cellulaires monoclonales stables qui sont compatibles avec les essais de routine, y compris le Western blotting, l'ELISA et l'immunohistochimie.
Q2: Comment l'immunogénicité peut-elle être réduite pendant le développement d'anticorps thérapeutiques?
R: L'immunogénicité peut être réduite de manière significative en passant du format murin aux formats d'anticorps monoclonaux chimériques, humanisés ou entièrement humains. Ces formats augmentent progressivement la proportion de séquence humaine dans l'anticorps, en réduisant le risque de développement d'anticorps anti-médicaments (ADA).
Q3: Quel est le calendrier typique pour la production d'anticorps monoclonaux de souris sur mesure?
R: Le développement d'anticorps monoclonaux de souris personnalisés comprend généralement l'immunisation animale, la détection du titre d'anticorps sériques, la fusion cellulaire, le sous-clonage et la purification des anticorps, et prend généralement plusieurs mois, en fonction du débit de dépistage et des exigences de validation.
Q4: Quelle quantité d'antigène est généralement nécessaire pour l'immunisation de la souris?
R: Typiquement, 300-500 μg d'antigène purifié est suffisant pour l'immunisation de 5 souris BALB/c dans des projets de développement d'anticorps monoclonaux personnalisés.
Q5: Le développement d'anticorps monoclonaux peut-il être intégré à d'autres essais de recherche?
R: Oui, le développement d'anticorps monoclonaux peut être parfaitement intégré aux technologies de soutien, y compris l'expression de protéines recombinantes, les kits ELISA, les kits d'essais biochimiques et les systèmes de coloration pathologique, formant un flux de travail de validation complet couvrant les applications de biologie moléculaire, de biologie cellulaire et d'immunologie.