せいちょうけいすう
分類と特徴
-
血小板由来成長因子(PDGF)
PDGFは2つのサブユニットからなり、A鎖(18 kDa)とB鎖(12〜14 kDa)と呼ばれ、同じ位置の8つの保存システイン残基を含む高度に相同性のペプチド配列を共有する。PDGFには3種類の亜型が存在する:相同二量体PDGF-AAとPDGF-BB、及び異二量体血小板源性成長因子-AB。これらの亜型は各種組織と細胞系に分布し、それぞれの亜型が異なる生物学的機能を持つことを表明した。
細胞表面にはPDGF受容体の2種類が存在する:PDGFR−αとPDGFR−β。PDGFR−αはPDGFのAおよびBサブユニットに結合することができ、PDGFR−βはBサブユニットに結合するだけである。PDGF−AAはαα受容体二量体と結合し、PDGF−ABはααとαβ二量体を形成することができ、PDGF−BBはαα、αβとβ受容体二量体を活性化することができる。これらの受容体二量体はPDGFRの活性信号形態を表す[1]。
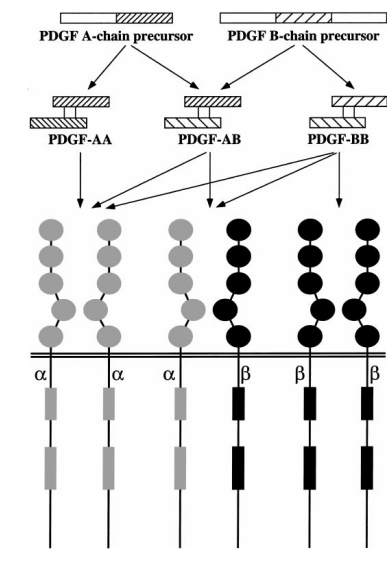
図1:血小板由来成長因子(PDGF)異性体の加工と機能[2]
-
血管内皮成長因子
血管内皮成長因子(VEGF)、血管透過性因子(VPF)とも呼ばれ、血管内皮細胞の高度に特異的な線維裂原である。VEGFファミリーには、VEGF-A、VEGF-B、VEGF-C、VEGF-D、VEGF-E、胎盤成長因子(PlGF)のいくつかのメンバーが含まれています。このうち、VEGF−Aは選択的mRNAスプライシングによって生成された4つの主要なサブタイプのうち、VEGF 121、VEGF 165、VEGF 189、VEGF 206に存在する。
VEGFは、3つの主要タイプのチロシンキナーゼ受容体を結合することにより、VEGFR−1(Flt−1)、VEGFR−2(Flk−1/KDR)、VEGFR−3(Flt−4)の生物学的効果を発揮する。各VEGFサブタイプはこれらの受容体に対して異なる結合親和性を示し、これはVEGFが媒介する信号経路の多様性に寄与する[3]。
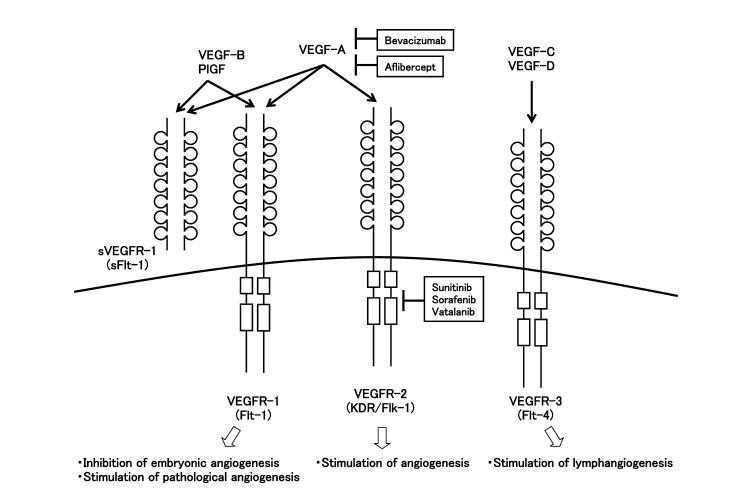
図2:VEGFファミリーメンバーとその受容体
VEGF−Aは一般的にVEGFと略称され、発育血管の生成、血管の生成、内皮前駆細胞の分化の鍵となる調節因子である。VEGF−Bは新生血管のない腫瘍に作用する。VEGF−CとVEGF−Dは腫瘍組織内の新しい血管とリンパ管の形成に関与している。VEGF−Eも潜在的な血管新生因子と考えられ、一方、PlGF(胎盤成長因子)は血管新生を促進し、血管透過性を高める。
-
表皮成長因子(EGF)
表皮成長因子(EGF)は人間や他の動物の体内に広く存在する小さなポリペプチドであり、50〜60個のアミノ酸のペプチド鎖からなる。この鎖は6つのシステイン残基を含み、安定したジスルフィド結合を形成し、その生物活性にとって重要な3つの環状ドメインを形成する。極めて低い濃度でもEGFは細胞成長を強力に刺激し、老化関連遺伝子の発現を抑制し、表皮細胞の老化を遅らせることができる。
EGFは、その受容体EGFR(表皮成長因子受容体)の細胞外領域(ドメインI-IVを含む)を結合することによって作用し、受容体チロシンキナーゼ二量化をもたらす[4]。この活性化は、細胞内のカルシウムレベルの上昇、サッカリン分解、タンパク質合成の増強、およびEGFR遺伝子自体を含むいくつかの遺伝子発現の増加を含む一連の生化学的事象を引き起こす。最終的に、これらの事象はDNA合成と細胞増殖を促進する。
-
線維芽細胞成長因子(FGF)
線維芽細胞成長因子(FGF)は、全身の様々な組織に存在するポリペプチド成長因子ファミリーである。それらは主にアルカリ性FGF(bFGF)と酸性FGF(aFGF)の2つの密接な関係の形で存在する。FGFファミリーは22個のリガンドからなり、4種類の異なるFGF受容体(FGFR)と相互作用することができる。FGF/FGFRシグナルパスは、細胞の生存、増殖、移動、分化、胚発育、器官発生、組織修復/再生、代謝などの基本的な細胞プロセスを制御する[5]。
名前“ ;線維芽細胞成長因子” ;線維芽細胞に対する強力な線維分裂促進作用を反映している。また、FGFは平滑筋細胞、軟骨細胞、角質形成細胞、周細胞の増殖を刺激する。ヘパリンに対する強い親和性から、FGFはヘパリン結合成長因子とも呼ばれる。これらは血管内皮細胞から合成され、基底膜と細胞外基質に貯蔵される。
-
インスリン様成長因子(IGFs)
インスリン様成長因子(IGF)ファミリーは、2種類の低分子量ポリペプチド(IGF−1及びIGF−2)、2種類の特定受容体(IGF−1 R及びIGF−2 R、I型及びII型受容体とも呼ばれる)及び6種類のIGF結合タンパク質(IGFBP)を含む。IGF−1 Rはインスリン受容体(IR)と構造的に類似しており、イソテトラマー糖タンパク質(α₂β₂) 2個のαサブユニットと2個のβサブユニットからなる。αサブユニットはリガンド結合ドメインを含み、βサブユニットは固有のチロシンキナーゼ活性を有する(ただし、チロシナーゼ活性はない)。
インスリンとIGFsとその受容体の結合親和性はそれぞれ異なる:
- インスリン受容体(IR)について:インスリン> ;IGF-1>;インスリン様成長因子-2
- IGF-1受容体(IGF-1 R)の場合:IGF-1> ;IGF-2>;インスリン
- IGF-2受容体(IGF-2 R)の場合:IGF-2> ;IGF−1、インスリンの交差反応は観察されなかった。
IGF−1は70アミノ酸からなる単鎖塩基性タンパク質であり、分子量は約7649 Daであり、顕著な熱安定性を有する。一方、IGF-2は67個のアミノ酸からなり、分子量は約7471 Daで、0.1%SDSで安定している単鎖微酸性タンパク質である。これら2つの遺伝子はヒトインスリン原と70%以上の配列相同性と約50%の構造的および機能的類似性を有する。
-
変換成長因子(TGFs)
形質転換成長因子(TGF−)とは、TGF−αとTGF−βの2種類のポリペプチド成長因子を指す。TGF−αはマクロファージ、脳細胞、表皮細胞から産生され、上皮発育の誘導に作用する。
人間において、TGF−βには3種類のサブタイプが存在する:TGF−β1、TGF−β2、TGF−β3。これらの異性体はTGF−β受容体I型(TGF−βR 1)とII型(TGF−αR 2)からなる共有受容体複合体と結合し、インビトロで類似の細胞内シグナルカスケードを誘導する[6]。
TGF−β(形質転換成長因子β)は多機能タンパク質であり、細胞成長、分化、アポトーシス、免疫調節を含む広範な細胞過程を調節する。TGF−β受容体はセリン/トレオニンキナーゼ受容体であり、下流信号伝導は主にSMAD経路及び/又はDAXX経路を介して媒介される。
-
結合組織成長因子(CTGF)
結合組織成長因子(CTGF)、FISP 12またはCCN 2とも呼ばれ、CCN蛋白質ファミリーに属し、Cyr 61、CTGF、Novの3つのメンバーを含む。これらのファミリーメンバーは高度なアミノ酸配列相同性を示し、4つの重要な構造領域を含む保守的な蛋白質構造を共有する:
- N−末端インスリン様成長因子結合ドメイン(IGFBP)、
- von Willebrand因子C型繰り返しシーケンス(VWC)、
- 血小板反応性蛋白1型反復配列(TSP 1)、
- およびシステインに富むC末端ドメイン(CT)を含む。
CTGFは1991年に初めて線維芽細胞誘導分泌蛋白質−12(FISP 12)と同定され、血清活性化NIH 3 T 3細胞から単離された。同年後半、「結合組織成長因子」という名称が提案された。
CTGFは当初、線維芽細胞の増殖、移動、接着、細胞外マトリックス(ECM)産生を促進する能力があると考えられていた。その各ドメインは特定のパートナータンパク質と結合し、CTGFが広範な生物学的機能を実行できるようにすることができる[7](図3参照)。
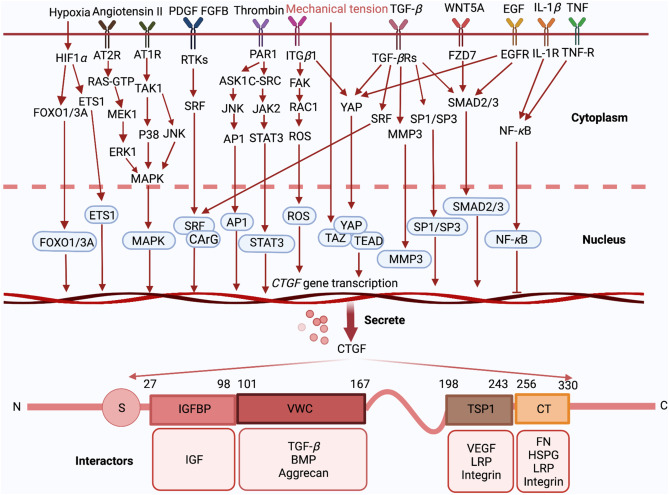
図3
外部刺激の下で、CTGF関連信号経路が活性化され、CTGF転写と分泌をもたらす。分泌後、CTGFの4つの異なるドメインであるIGFBP、VWC、TSP 1、CTは、さまざまな分子と相互作用し、その生理機能を発揮することができる。
-
角質細胞成長因子(KGF)
角質細胞成長因子(KGF)は皮下組織間葉質細胞分泌の基本タンパク質成長因子である。それは特に上皮細胞の様々な生理過程を刺激し、代謝、再生、分化、移動を含む。KGFは人体内に天然に存在する、生物活性を有する可溶性タンパク質であり、194個のアミノ酸配列によってコードされる。KGFの成熟形態は163個のアミノ酸残基からなり、N末端グリコシル化部位を含む。
KGFは主に皮下組織から分泌され、上皮細胞表面の受容体と特異的に結合する。複雑なシグナルカスケードにより、細胞分裂と成長に関与する遺伝子の発現を活性化し、上皮組織の代謝活動と再生を促進する。
-
神経成長因子(NGF)
神経成長因子(NGF)ファミリーには、NGF自体、脳源性神経営養因子(BDNF)、神経営養因子−3(NT−3)、神経成長因子−4/5(NT−4/5)、および小さい程度では、神経営養因子−6と神経栄養因子−7といういくつかの神経営養因子が含まれる。その中で、前の4つは最も際立っていて、研究が最も深いです。
NGFはこの家族の中で最も重要で代表的なメンバーです。組織において、NGFは主に前駆体形態で存在し、主に顎下腺中で成熟形態に加工される。NGFはニューロンの生存を支持し、神経を保護し、神経再生を促進し、免疫反応を調節し、傷口の癒合を促進し、腫瘍の成長を抑制するなど、様々な作用を有する。
上記の成長因子に加えて、他の重要なメンバーには、IL−1およびIL−3などのインターロイキン関連成長因子、エリスロポエチン(EPO)、およびコロニー刺激因子(CSF)が含まれる。これらの分子は、さまざまな生理的および病理的環境における細胞増殖、分化、免疫反応を調節する上でも重要な役割を果たしている。
作用メカニズム
-
さようモード
内分泌:成長因子は血液分泌と輸送を通じて、遠くの標的細胞に作用する。一例は血小板由来成長因子(PDGF)である。
傍分泌:細胞分泌の成長因子は近くの異なるタイプの細胞に作用し、それらの行動に影響を与える。
自己分泌:成長因子はそれらを合成し分泌する同じ細胞に作用する。
その中で、傍分泌と自己分泌信号はほとんどの成長因子の主要な作用方式である。
-
機械的経路
様々な細胞型から分泌された後、増殖因子(GF)は標的細胞の表面または内部に位置する特定の受容体と結合することによってその生物学的役割を果たす。リガンド結合後、これらの受容体は細胞内シグナルカスケードを活性化し、対応する生物反応を媒介する。
1つの主要な成長因子受容体は、受容体チロシンキナーゼ(RTK)と呼ばれる固有のチロシンキナーゼ活性を有する。RTKは、表皮成長因子受容体(EGFR)ファミリー、血小板由来成長因子受容体、神経成長因子受容体を含む約20のファミリーに分類される。ほとんどの成長因子の役割はRTKによって媒介される(図4参照)。
成長因子が細胞表面の受容体と結合すると、RTKの二量化とその後のキナーゼドメインの活性化がシグナル伝達を開始する。RTK二量体中の2種類のモノマーはチロシン残基上で交差リン酸化し、受容体を完全に活性化する。RTK C末端尾部のこれらのリン酸化チロシン残基は、複数の下流信号分子の接合部位として機能する。
これらのRTK信号複合体の形成は、Ras/Erk、PI 3 K/Akt、Src/Jak/Stat、PLC-γ1パスを含む様々な下流信号パスの活性化をもたらす。これらの経路は相互作用し、複雑な信号ネットワークを形成する[8]。
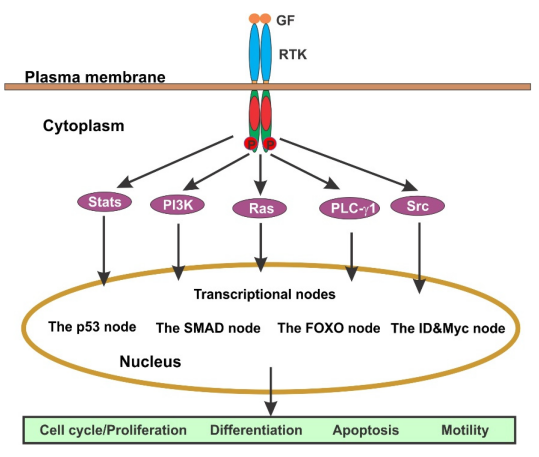
図4
RTK-Ras信号経路:
リガンド結合→ 受容体チロシンキナーゼ(RTK)の活性化→ 活性化RTK募集アダプター蛋白質→ グアニンヌクレオチド交換因子(GEF)はGDP放出を促進する→ Ras(GTP結合タンパク質)の活性化。
このアクティブ化により、一連のダウンストリームイベントがトリガーされます。
活性化されたRasはRafの活性化を開始し、Rafはセリン/トレオニンタンパク質キナーゼ(MAPKKKKとも呼ばれる)であり、標的タンパク質上のセリン/トレオニン残基をリン酸化することができる→ 活性化されたRafはMAPK(MAPKキナーゼ)を結合しリン酸化し、活性化をもたらす。MAPKKは二重特異性キナーゼであり、MAPK上のトレオニンとチロシン残基をリン酸化し、MAPKを活性化することができる→ 活性化されたMAPKは細胞核に転位する→ 他のキナーゼまたは遺伝子調節タンパク質(すなわち転写因子)のリン酸化、遺伝子発現の調節(図5参照)。
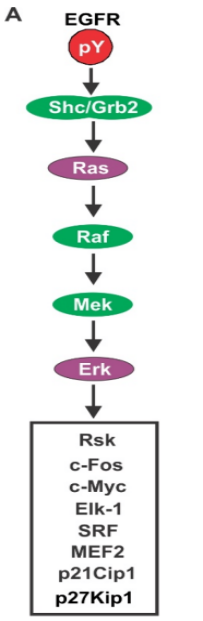
図5
参考文献
1 Kaji K.血小板源性成長因子の機能、分子構造及び遺伝子発現制御。日本林修1992年8月、50(8):1902-1909.
2 Heldin CH,Westermark B.血小板由来成長因子の作用機序とinvivo作用。《生理学評論》1999年10月、79(4):1283-1316.
3 Takahashi S.血管内皮増殖因子(VEGF)、VEGF受容体及びその阻害剤の抗血管形成腫瘍治療への応用。バイオ製薬牛。 2011;34(12):1785-1788.
4 Ogiso H、Ishitani R、Nureki O、など。ヒト表皮成長因子と受容体細胞外領域複合体の結晶構造。細胞。2002年9月20日、110(6):775-787.
5 Mossahbi-Mohammadi M、Quan M、Zhang JS、など。線維芽細胞成長因子シグナルパス:幹細胞多能性の鍵となる調節因子。前細胞開発生物学。2020年2月18日、8:79.
6孫T、範海登JA、高X、等.系硬化症によるTGF-β3異性体の選択的抑制作用。医学2024年2月9日、5(2):132-147.e7。
7感作、彭、蘭、など。多機能調節蛋白結合組織成長因子(CTGF):多種疾患の潜在的治療標的。薬物学報B.2022年4月、12(4):1740-1760.
8王Z.成長因子誘導細胞シグナルによる細胞周期プロセスの調節。細胞2021、103327。
関連製品:
詳細については、お店のWebサイトを参照してください。 www.solarbio.com.
|
猫号。 |
製品名 |
猫号。 |
製品名 |
|
SEKH-0052 |
ヒトVEGF ELISAキット |
SEKH-0050 |
ヒトEGF ELISAキット |
|
土曜日-0316 |
ヒトTGF−β1 ELISAキット |
SEKM-0035 |
マウスTGF-β1 ELISAキット |
|
SEKM-0039 |
マウスVEGF ELISAキット |
SEKR-0032号 |
ラットVEGF ELISAキット |
|
SEKR-0010 |
ラットEGF ELISAキット |
SEKR-0012号 |
ラットTGF-β1 ELISAキット |