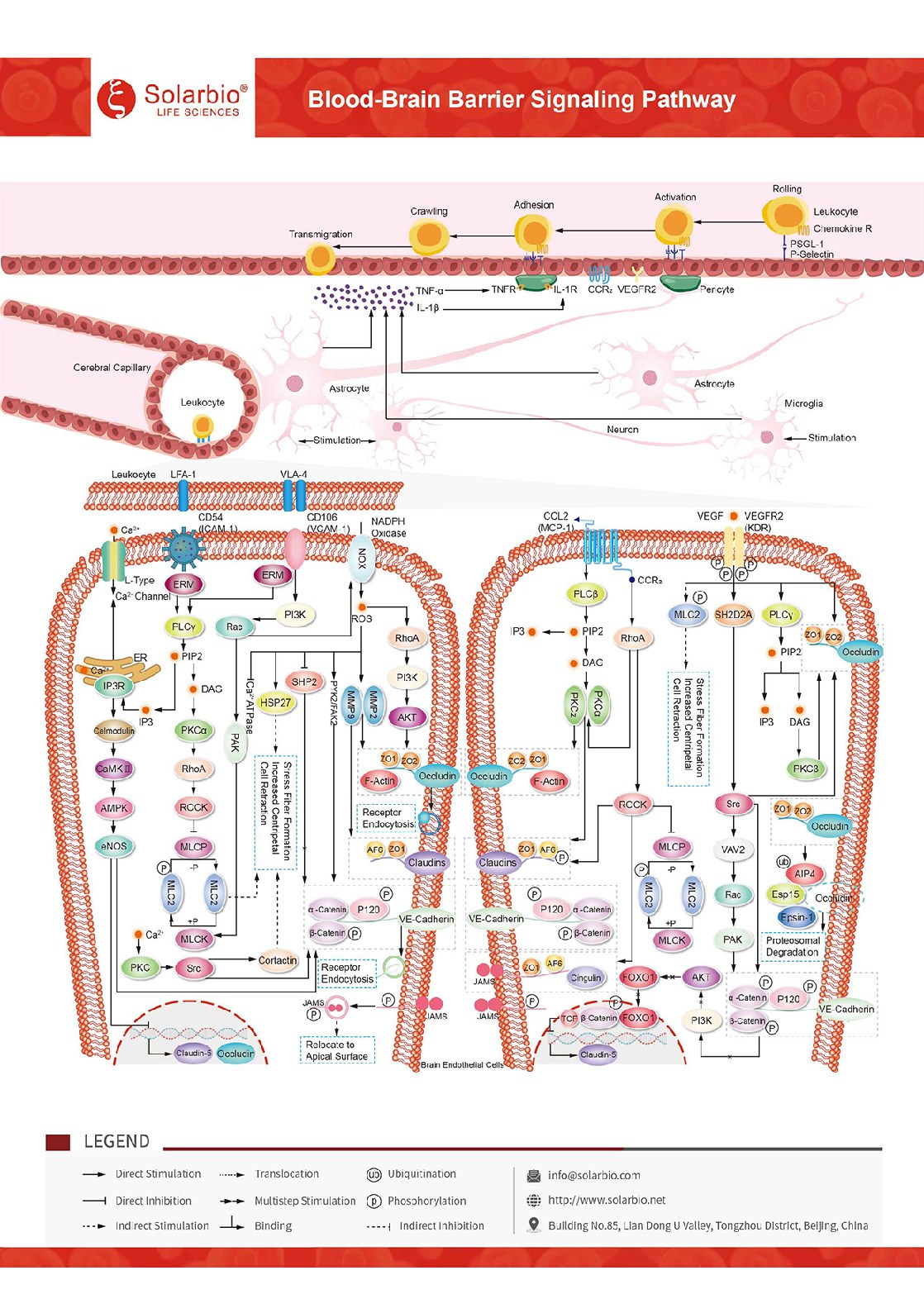
Кровно-мозговый барьерный сигнальный путь
Кровомозговый барьер является прочным барьером внутри мозговой микровоскулары. Он включает в себя физический барьер, состоящий из специализированных эндотелиальных клеток (ЭК), состоящих из апикальных тесных соединений (TJ), средних адхезирующих соединений (AJ) и средних базолатеральных Ca.2+зависимые адхезии, а также метаболический барьер, поддерживаемый ферментами и белками оттока насоса. Вместе они образуют высокоселективный диффузионный барьер между периферической циркуляцией и центральной нервной системой (ЦНС). Химокин CCL2/MCP-1 является ключевым химокином, регулирующим миграцию и инфильтрацию моноцитов/макрофагов. В центральной нервной системе в состоянии нейропаления CCL2/MCP-1 увеличивается и связывается с рецептором CCR2, связанным с белком G, на ЭК мозга. Индуцируя фосфорилирование белков TJ, CCL2/McP-1 инициирует внутриклеточный сигнальный каскад для дезинтеграции и/или перераспределения белков TJ с края клетки, вызывая динамическую реорганизацию соединительных комплексов и сокращение ЭК. Белки JAM будут переориентироваться на апикальную поверхность эндотелиальных клеток и участвовать в адгезивных взаимодействиях с лейкоцитными интегринами. Молекула межклеточной адгезии-1 (ICAM-1/CD54) Ig-подобный адгезионный рецептор, который связывается с лейкоцитным интегрином αLβ2 (LFA-1), индуцирует агрегацию ICAM-1/CD54 и активацию внутриклеточных сигнальных путей, включая киназы семьи Src и пути Rho/ROCK. Кроме того, сигнализация ICAM-1/CD54 способствовала эндоцитозу окклудина и VE-кадерина. Молекула адгезии сосудистых клеток-1 (VCAM-1/CD106) является Ig-подобным адгезионным рецептором и лигандом для лейкоцитного интегрина α4β1 (VLA-4). Агрегация VCAM-1/CD106 и активация внутриклеточных сигнальных путей, которые индуцируют фосфорилирование белка TJ, приводят к демонтажу и/или перераспределению белков TJ с края клетки, которые в свою очередь посредничествуют в миграционном процессе лейкоцитов из эндотелия в ткани через кровообращение. Кроме того, сигнализация VCAM-1/CD106 способствует производству матричных металлопротеиназ (MMP), которые деградируют коннексин. VEGF является высокоспецифическим прососудистым фактором роста эндотелиальных клеток. В состоянии нейропаления VEGF повышается в ЦНС, связывается с рецепторами на ЭК мозга и инициирует внутриклеточные сигнальные каскады, которые возникают, вызывая динамическую реорганизацию соединительных комплексов и сокращение ЭК. VEGF способствует эндоцитозу окклудина и VE-кадерина. Альтернативно, VEGF индуцирует деградацию окклудина через путь убиквитина-протеазомы. VEGF также может снижать экспрессию окклудина и клаудина-5. В нормальных условиях специализированная структура БББ предотвращает параклеточный транспорт большинства гидрофилных соединений через эндотелиальные клетки мозга и ограничивает миграцию клеток крови в центральную нервную систему. В процессе нейропаления соединительные комплексы, такие как TJ и AJ, могут быть переформированы, чтобы образовать эндотелиальные пробелы, через которые периферические иммунные клетки войдут в центральную нервную систему (ЦНС). Сигналы CCL2/MCP-1, ICAM-1/CD54, VCAM-1/CD106 и VEGF могут вызывать реорганизацию микронитей F-актина в стрессовые волокна, тем самым увеличивая центротропное напряжение в клетках и приводя к сокращению клеток. Продолжительное повреждение ткани может вызвать воспаление и вызвать потерю ограничивающей функции гемато-мозгового барьера. Реактивные микроглии, астроциты, перициты и эндотелиальные клетки выделяют большое количество молекул (таких как CXCL8 / IL-8, CCL2 / MCP-1, TNF-α, IL-1beta / IL-1F2 и т. д.), что приводит к повышению сосудистой проницаемости. Он способствует вторжению периферических иммунных клеток в центральную нервную систему. Как сообщалось, дисфункция кровеномозгового барьера и последующее увеличение инфилтрирующих иммунных клеток связаны с различными неврологическими заболеваниями, включая Альцгеймера; с болезнь, Паркинсон’ болезни и рассеянного склероза.